
题目列表(包括答案和解析)

 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH-

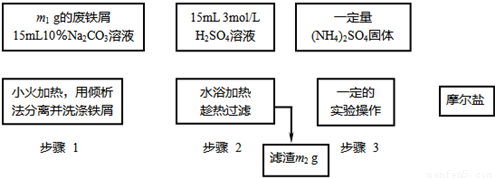
硫酸亚铁铵的制备
1、硫酸亚铁铵晶体的性质
物理性质:浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO4和(NH4)2SO4都要小
化学性质:能水解;具有还原性,但比硫酸亚铁稳定
2、将绿矾(FeSO4•7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体。
(NH4)2SO4+FeSO4+ 6H2O= (NH4)2SO4•FeSO4•6H2O↓根据下图回答:
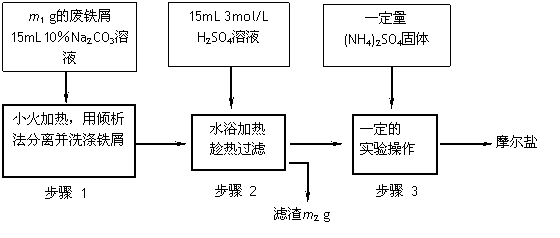
(1)步骤1Na2CO3的主要作用是 。
(2)步骤2中铁屑过量的目的是(用离子方程式表示):
(3)步骤3中,加入(NH4)2SO4固体后,要得到摩尔盐晶体,需经过的实验操作包括:加热蒸发、 、 。
(4)步骤3中制得的晶体过滤后用无水乙醇洗涤的目的是 。
操作对比:
1、三个步骤中都含有加热的操作:
步骤1中:小火加热的目的是:
;
步骤2中:水浴加热的优点是 ;
水浴加热是为了 ;
步骤3中:加热是为了蒸发溶剂,浓缩结晶。
思考:该实验中,要得到摩尔盐晶体,应加热到 时,停止加热。
为什么不能蒸干?
那么蒸发下列溶液呢?
①从CuSO4溶液得到胆矾晶体: 。
②从NaCl溶液得到NaCl固体:
2、三个步骤中都含有固液分离的操作:
步骤1中采用倾析法分离出铁屑,下列适合用倾析法的有:
A、沉淀的颗粒较大 B、沉淀容易沉降
C、沉淀呈胶状 D、沉淀呈絮状
步骤2中溶液趁热过滤的原因是 。
步骤3中可以用如下装置进行过滤: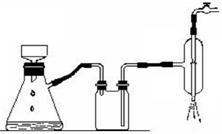
(1)这种过滤方式称为:
(2)这种过滤跟普通过滤相比,除了过滤速度快外,
还有一个优点是: 。
(3)你能讲出仪器A、B、C的名称么?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com