
题目列表(包括答案和解析)
关于下列四个图像的说法中正确的是
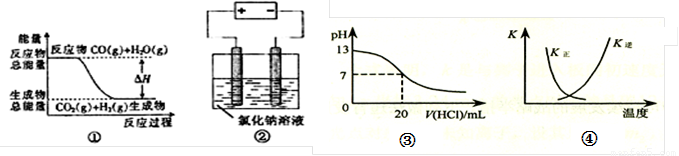
 A.图①表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)中的△H大于0
A.图①表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)中的△H大于0
B.图②是石墨为电极电解氯化钠稀溶液,阴、阳两极产生气体体积之比一定为1:1
C.图③表示25℃,0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,pH随加入酸体积的变化
D.图④表示2SO2(g) + O2(g)  2SO3(g)
ΔH < 0 正、逆反应平衡常数K随温度的变化
2SO3(g)
ΔH < 0 正、逆反应平衡常数K随温度的变化
关于下列四个图像的说法中正确的是

A.图①表示可逆反应“CO(g)+H2O(g)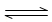 CO2(g)+H2(g)”中的△H大于0
CO2(g)+H2(g)”中的△H大于0
B.图②是在以石墨为电极电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.图④中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
关于下列四个图像的说法中正确的是
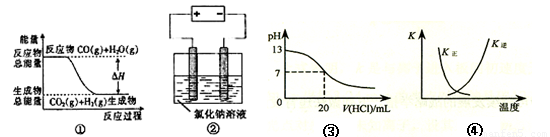
A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
CO2(g)+H2(g)”中的△H大于0
B.图②是在以石墨为电极电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1
C.图③表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
D.图④中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
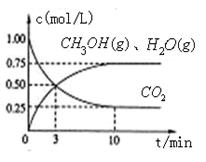
 。
。 0(填“>”“<”或“=”)。
0(填“>”“<”或“=”)。| A.升高温度 | B.充入氮气 | C.将水蒸气从体系中分离 | D.用更有效的催化剂 |
 2SO3(g) ΔH=" —196.6" kJ·mol―1
2SO3(g) ΔH=" —196.6" kJ·mol―1 2NO2(g) ΔH= —113.0 kJ·mol―1
2NO2(g) ΔH= —113.0 kJ·mol―1 SO3(g) + NO(g) 的ΔH= 。
SO3(g) + NO(g) 的ΔH= 。 2SO3(g) ΔH=-92.3KJ/mol
2SO3(g) ΔH=-92.3KJ/mol 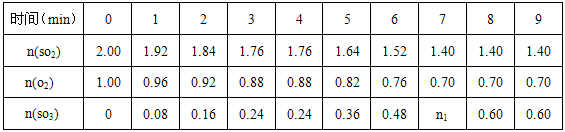


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com