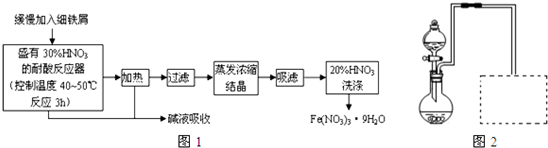
Fe、Cu都是人类最早使用的金属,某化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题
:(1)甲同学取两束细铜丝用砂纸打磨后在酒精灯上灼烧至红热,再分别迅速伸入盛满O
2或Cl
2的两个集气瓶中.其中能看到燃烧现象的集气瓶中所装气体是
Cl2
Cl2
.
(2)乙同学为验证Fe在冷的浓HNO
3中发生钝化,但能和热的浓HNO
3反应,设计了如图所示的实验,请你指出其中的两处主要错误:①
;②
加热液体的试管应与桌面成45°角向上倾斜
加热液体的试管应与桌面成45°角向上倾斜
纠正上述错误后,如将装置2中的铁片改成一段一端为螺旋状的铁丝,呈螺旋状的一端深人硝酸中,另一端伸出橡皮塞外,这种改进的优点是
既能控制反应的进行又能减少氮氧化物的排放
既能控制反应的进行又能减少氮氧化物的排放
.
(3)丙同学将乙同学的Fe和浓HNO
3反应后的溶液冷却,再将溶液倒人烧杯中并加入一块Cu片,发现Cu片逐渐溶解.
①丙同学依据反应中某一现象得出了乙同学实验后HNO
3过量的正确结论,他依据的反应现象是
试管上部出现红棕色气体
试管上部出现红棕色气体
.
②丙同学认为铜片溶解可能还有另一化学反应的存在原因,该反应的离子方程式是
2Fe3++Cu=Cu2++2Fe2+
2Fe3++Cu=Cu2++2Fe2+
(4)丁同学取0.05molOi与足量浓HNO
3反应,采用了正确的试验方法,但收集产生的气体不足0.1mol,最有可能的原因是(用化学方程式表示)
2NO2?N2O4
2NO2?N2O4
.



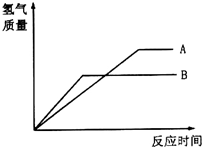 等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:
等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示: