
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)

| ||
| ||
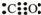
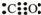
 F ЃЈgЃЉ+D ЃЈgЃЉЗДгІЫйТЪКЭЪБМфЕФЙиЯЕШчЭМ2ЫљЪОЃЌФЧУДдкt1ЪБЫйТЪЗЂЩњИФБфЕФдвђПЩФмЪЧЃЈЬюбЁЯюзжФИЃЉ
F ЃЈgЃЉ+D ЃЈgЃЉЗДгІЫйТЪКЭЪБМфЕФЙиЯЕШчЭМ2ЫљЪОЃЌФЧУДдкt1ЪБЫйТЪЗЂЩњИФБфЕФдвђПЩФмЪЧЃЈЬюбЁЯюзжФИЃЉ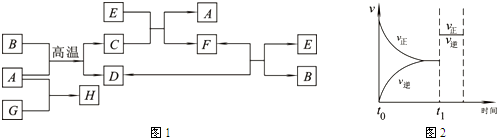
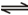 F ЃЈgЃЉ+D ЃЈgЃЉЗДгІЫйТЪКЭЪБМфЕФЙиЯЕШчЭМ2ЫљЪОЃЌФЧУДдкt1ЪБЫйТЪЗЂЩњИФБфЕФдвђПЩФмЪЧЃЈЬюбЁЯюзжФИЃЉ______ЃЎ
F ЃЈgЃЉ+D ЃЈgЃЉЗДгІЫйТЪКЭЪБМфЕФЙиЯЕШчЭМ2ЫљЪОЃЌФЧУДдкt1ЪБЫйТЪЗЂЩњИФБфЕФдвђПЩФмЪЧЃЈЬюбЁЯюзжФИЃЉ______ЃЎАйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com