
题目列表(包括答案和解析)
(15分)乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为 。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯

某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是 。
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止 。
③相关物质的部分性质:
| | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |

| ||
| ||


 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 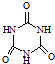 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
有
M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
(1)在A、B、D、E四种元素的最简单氢化物中,沸点最高的是
________(填化学式).M、D、E、N形成的简单离子的半径由大到小的关系是(写元素符号)________.
(2)A、B、D、M可组成多种18电子分子,请写出2种具有18电子的有机物的分子式(用元素符号表示)________、________.
(3)由A、D、N三种元素组成的无机物(相对分子质量106),其水溶液呈碱性,用离子方程式表示其原因________.
(4)元素B的氢化物与元素D单质在一定条件下发生置换反应,在该反应中氧化剂与还原剂的物质的量之比为________.
(5)由D、N形成的原子个数1∶1的化合物的电子式为________.其中包含的化学键类型有________和________.
(6)NH3·H2O的电离方程式为NH3·H2O![]() NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是:________(填“a”或“b”)
NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是:________(填“a”或“b”)

太湖、巢湖、滇池是我国重点治理的三大湖,三大湖受到严重的富营养化污染,藻类疯狂繁殖,破坏了生态平衡,影响了人民的健康,必须迅速进行治理。请回答:
(1)藻类的狂长,说明水中哪些元素超标? 这些元素从哪里引入的?
(2)您认为引起藻类大量繁殖最主要的是哪一种元素? 以什么形态出现? 请你设计一个测定此元素的方法。
(3)水质污染程度的重要标志之一为BOD(生物化学耗氧量),它是指由于水中微生物的繁殖或呼吸作用,或水中有机物分解时所消耗的溶解氧的量,单位为mgO2/L。现有巢湖沿岸某电镀厂,不遵守环境法规,每周向湖中排放一次含氰废水,使近岸湖水含CN-的浓度为7.5×10-5mol/L,CN-与O2作用生成CO2、N2等。试问此电镀厂每排放一次废水将使近岸湖水的BOD增大多少?
(4)水质污染程度的另一重要指标为COD(化学耗氧量),它是指水中还原性物质(有机的和无机的),在规定条件下被氧化时,1L水样所消耗的氧的毫克数。测定COD通常有KMnO4法、K2Cr2C7法等。酸性KMnO4法:KMnO4在酸性溶液中经沸水浴加热,将发生:
2KMnO4+3H2SO4==K2SO4+2MnSO4+3H2O+5[O]。
①若为0.01000mol/L KMnO4溶液,则1.00mL相当于 mgO2;
②若巢湖水样100mL,加入1:2 H2SO410mL,AgSO41g,混匀后,又加10mL 0.01000mol/L KMnO4溶液,在沸水中加热30min,取出加入10mL 0.02500mol/L Na2C2O4溶液,立即用0.01000mol/L KMnO4滴至微红色在15秒内不变色为终点,耗KMnO4液7.00mL,求巢湖水样的COD为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com