
题目列表(包括答案和解析)
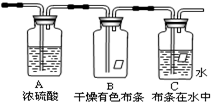
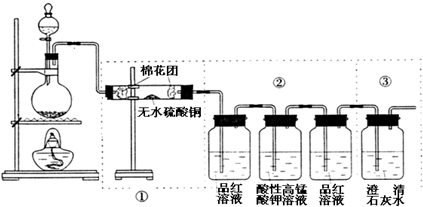
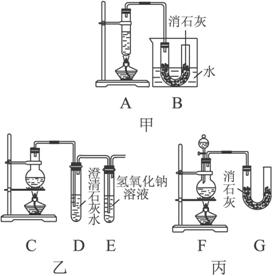
(1)有下列几项优缺点:a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。请从上面对图所示的甲、乙、丙三套装置的优缺点作出评析,选择符合题目要求的选项填在下列空格内。
| 优点 | 缺点 |
①甲装置 |
|
|
②乙装置 |
|
|
③丙装置 |
|
|
(2)如所示装置中,甲由A、B两部分组成;乙由C、D、E三部分组成;丙由F、G两部分组成。请从图A—G各部分装置中选取合理的组成部分,组装成一套较完善的实验装置,装置的连接顺序(按气流从左到右的方向)是____________。
(3)实验中若用100 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是(填“大于”“小于”或“等于”)0.15 mol,其原因是(假定各步反应均无反应物损耗,且无副反应发生)_____________________________________________________。
Ⅰ.卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性
质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
|
步骤 |
现象 |
|
ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 |
随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
|
ⅱ.继续向上述溶液中滴入KBrO3溶液 |
溶液的蓝色逐渐褪去 |
请回答:
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(2)若用y表示锥形瓶中含碘物质的物质的量 ,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。
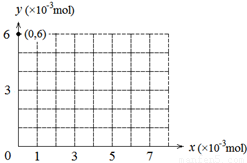
Ⅱ.过碳酸钠中含有少量过氧化钠,甲、乙两位同学各称取一定质量的该样品,并用如下图所示仪器测定样品的纯度。仪器的连接顺序:
甲同学:⑤—⑧—③—⑦—④; 乙同学:⑤—③—②。

已知:过碳酸钠(Na2CO4)、过氧化钠分别跟足量稀硫酸反应的化学方程式如下:
2Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O;
2Na2O2+2H2SO4=2Na2SO4+O2↑+2H2O。
(1)甲同学想通过实验测得的数据是____________,他选用的装置________(填序号)是没有必要的。
(2)乙同学想通过实验测得的数据是________________。有人认为按他测得的数据计算出的实验结果可能偏高,原因是________________; 为了测得准确的实验数据,请你将乙同学的实验设计进行改进,写出你所选用仪器的连接顺序(每种仪器最多使用一次,也可以不用):________________(填序号)。
有如下图所示六组制取漂白粉的装置,请依据题意回答问题。
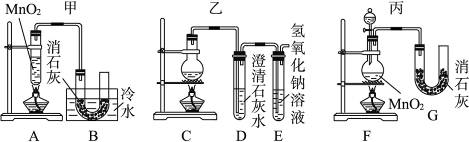
(1)有下列几项优缺点:a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。请对上图所示的甲、乙、丙三套装置的优缺点作出评析,选择符合题目要求的选项填在下列空格内。
| 优点 | 缺点 | |
| ①甲装置 | ||
| ②乙装置 | ||
| ③丙装置 |
(2)上图所示装置中,甲由A、B两部分组成;乙由C、D、E三部分组成;丙由F、G两部分组成。请从图A~G各部分装置中选取合理的组成部分,组装成一套较完善的实验装置,装置的连接顺序(按气流从左到右的方向)是__________。
(3)实验中若用100 mL 12 mol·L-1 的浓盐酸与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是__________(填“大于”“小于”或“等于”)0.15 mol,其原因是(假定各步反应均无反应物损耗,且用无副反应发生)________________________________________。
(5分)解释钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀; B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球; D.钠不断与水反应;
E.生成的氢氧化钠使酚酞试液变红。
请在下表填写与描述的现象相对应的原因。
实验现象 | 原因(填以上序号) |
钠浮在水面上 |
|
熔成闪亮的小球 |
|
小球向各个方向迅速游动,并发出“嘶嘶”的声音 |
|
小球逐渐变小最后完全消失 |
|
在反应后的溶液中滴入酚酞试液显红色 |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com