
题目列表(包括答案和解析)
现有六种短周期元素A、B、C、D、E、F,其原子序数逐渐增大,其中B与C、D与F分别位于一周期,A与D、C与F分别位于同一主族,且A、D两元素原子的质子数之和是C、F两元素原子质子之和的一半,又知六种元素所形成的常见单质在常温常压下三种是气体,三种是固体.请回答下列问题:
(1)B元素单质的电子式为________,F元素氧化物的晶体类型为________.
(2)由A、C两元素可组成X、Y两化合物,X在MnO2作用下可以分解生成Y,写出该反应的化学方程式________.
(3)若E是非金属元素,其单质能表现出某些金属单质的物理性质,写出E与D的氧化物的水溶液反应的离子方程式________.
(4)一定条件下,A的单质与B的单质充分反应生成6.8 g W气体时,可放出18.48 kJ的热量,写出该反应的热化学方程式________.
(5)B、C、F的氢化物的热稳定性由强到弱的顺序为________.(填化学式)
| A、只有一种元素组成的物质一定是纯净物 | B、分子晶体溶于水时,一定不破坏共价键 | C、胶体产生丁达尔效应是由粒子的大小决定的 | D、同位素的质量数不同,物理性质不同;同位素不同原子构成的单质的化学性质也不相同 |
| ① | ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||||
| ⑦ | ⑩ | |||||||||||||||||||
| ⑾ | ⑧ | ⑨ | ||||||||||||||||||
 Be(OH)2+2HCl
Be(OH)2+2HCl Be(OH)2+2HCl
Be(OH)2+2HCl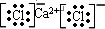
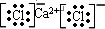
(本小题满分14分)a、b、c、d、e四种短周期元素的原子序数逐渐增大。a为非金属元素,且a、e同主族,c、d为同周期的相邻元素。e原子的质子数等于c、d原子最外层电子数之和。b原子最外层电子数是内层电子数的2倍。c的氢化物分子中有3个共价键。试推断:
(1)写出b元素在周期表中的位置 ;
(2)有a、c、d所形成的离子化合物是 它与e的最高价氧化物对应水化物的溶液加热时反应的离子方程式是 ;
(3)c的单质的电子式为 。
(4)b和d相比,非金属性较强的是 (用元素符号表示),下列事实能证明这一结论的是 (选填字母序号)。
| A.常温下,b的单质呈固态,d的单质呈气态 |
| B.d的氢化物的稳定性强于b的氢化物 |
| C.b与d形成的化合物中,b呈正价 |
| D.d的氢化物的沸点高于b的氢化物 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com