水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
(1)下列“水”中属于纯净物的是
C
C
.
A.矿泉水 B.雨水 C.蒸馏水 D.自来水
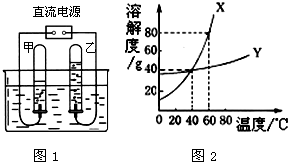
(2)如图1是电解水的实验装置,甲试管中收集到的气体是
氢气
氢气
.
(3)我国生活饮用水的主要标准为:
| 感官指标 |
化学指标 |
细菌指标 |
| 水质无色无味澄清 |
PH:6.5~8.5 |
细菌总个数<100个/mL等 |
要得出化学指标,测定表中的数值能否
不能
不能
(填“能”或“不能”)使用PH试纸,要使水的感官指标更好,可用利用
活性炭
活性炭
(填物质名称)来净化水.
(4)水常用作溶剂.公共场所可用过氧乙酸溶液对环境消毒.现有溶质质量分数为15%的过氧乙酸溶液10g,要配制成溶质质量分数为1%的过氧乙酸溶液,需加水
140
140
g.
(5)如图2,X、Y两种固体物质在水中的溶解度曲线图.
①60℃时,把45g的X加入50g水中,充分溶解,得到该温度下X的水溶液是
饱和
饱和
(填“饱和”或“不饱和”)溶液.
②在40℃时,分别将100gX的饱和溶液和200gY的饱和溶液蒸发掉10g水,析出晶体的质量分别为mg和ng,则m
=
=
n(填“>”、“=”或“<”).
(6)用水鉴别物质有一定规律,掌握其规律会使学习更轻松.现有四种白色固体,分别是NaOH、CuSO
4、NaCl、CaCO
3,只提供蒸馏水,将其鉴别开.
①根据是否溶于水和溶于水时形成蓝色溶液,可分别鉴别出
CuSO4和CaCO3
CuSO4和CaCO3
;
②将溶于水时形成的无色溶液的两种物质分为一组,根据溶液温度
升高
升高
(填“升高”、“降低”或“不变”),可鉴别出
NaOH
NaOH
.
(7)我市陆良的铬渣污染,主要是重金属铬对水源的污染.镉的化合物氯化镉(CdCl
2)也是污染水源的重金属之一,为消除污染,处理方法之一就是加入烧碱,发生复分解反应生成镉的化合物沉淀下来,请写出氯化镉(CdCl
2)与烧碱反应的方程式:
2NaOH+CdCl2=2NaCl+Cd(OH)2↓
2NaOH+CdCl2=2NaCl+Cd(OH)2↓
.
(8)节假日或双休日,去郊游野炊实为一大快事.然而,在野炊的情趣之中,如果遇到下面一些问题,你是如何怎么处理的?
①野餐食谱如下:主食:馒头 配菜:烤火腿、鲫鱼汤、五香豆干.从营养角度来看,你准备再添-样
C
C
;(填字母)A.炒鸡蛋 B.牛奶 C.黄瓜
②郊外通常比较泥泞,如果你的交通工具是自行车,你回来进行清洗后是如何防锈的:
AB
AB
.(填字母)
A.立即晾晒干 B.链条传动部件涂上油 C.涂油漆.


 水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
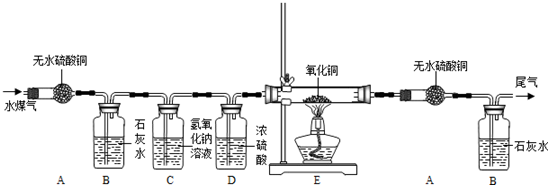
 科学探究是重要的学习方式,假设和验证是探究过程中的重要环节.为了探究“铁丝可 以在纯净的氧气中燃烧”,同学们将一根火柴梗塞入一段螺旋状“铁丝”(可能是纯铁铁丝或含碳铁丝)末端,将它固定,用镊子夹住“铁丝”,然后将火柴在酒精灯上点燃,将“铁丝”由集气瓶口向下慢慢伸入,观察现象:
科学探究是重要的学习方式,假设和验证是探究过程中的重要环节.为了探究“铁丝可 以在纯净的氧气中燃烧”,同学们将一根火柴梗塞入一段螺旋状“铁丝”(可能是纯铁铁丝或含碳铁丝)末端,将它固定,用镊子夹住“铁丝”,然后将火柴在酒精灯上点燃,将“铁丝”由集气瓶口向下慢慢伸入,观察现象: