
题目列表(包括答案和解析)
下图中A、B、C是常见的化学实验装置,请回答下列问题:
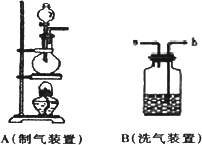
(1)实验里用A装置加热可制取氯气,为得到纯净干燥的氯气,可让A中逸出的气体在进入收集装置前依次通过分别装有________和________的两个洗气瓶B,此时应从B装置中的________(填a或b)口通入气体.
(2)铜在氯气中剧烈燃烧,使集气瓶充满________色的________(填烟或雾),有关化学方程式为________;
(3)为防止氯气尾气污染空气,可用________溶液吸收多余的氯气,原理是(用离子方程式表示)________.
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,工业上生产漂白粉的化学方程________.漂白粉的主要成分是________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体主要是________(用字母代号填).
A.O2
B.Cl2
C.CO2
D.HClO
如图中A、B、C是常见的化学实验装置,请回答下列问题:
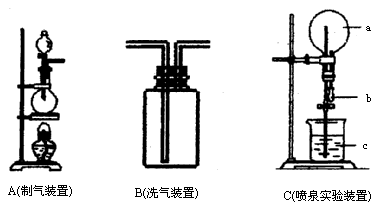
(1)利用A装置,当不加热时,可制取的一种气态单质是________;当加热时,可制取的一种化合物是________.
(2)化学实验室用A装置加热制取氯气,化学方程式为:
________.
为得到纯净、干燥的氯气,可让A中出来的气体在进入收集装置前依次通过分别装有________和________的两个洗气瓶B.
(3)实验室制取氯气和二氧化碳都可用瓶口向上排空集气法收集,具体操作有何不同?为什么?
________
(4)有一烧瓶纯净、干燥的氯气,用装置C做喷泉实验,如何操作才能形成喷泉?
________.
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。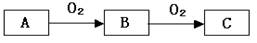
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,试用化学方程式表示该物质与二氧化碳气体的反应 。将C长期露置于空气中,最后将变成物质D,D的化学式为 。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
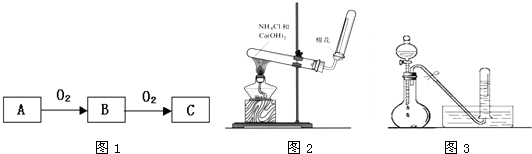
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题: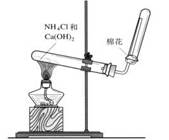
①收集A的方法是 ,验证A是否已经收集满的方法是 (任写一种)。
②写出实验室制取A的化学方程式 。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
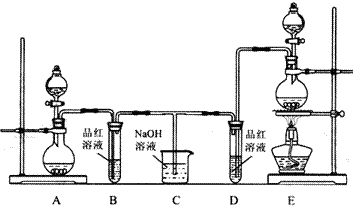
④试写出C与水反应的化学方程式 ,反应可得到酸X,X是 电解质(填“强”或“弱”)。如下图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式 。实验完毕后,试管中收集到的气体的主要成分为 (写化学式)。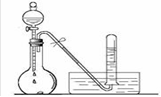
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com