
题目列表(包括答案和解析)
如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失)。
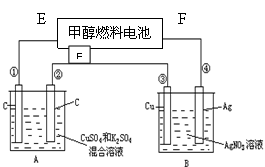
请回答下列问题:
(1)分别指出F电极、②电极的名称
、 。
(2)④电极的反应式: 。
E电极的反应式: 。
①电极上产生的实验现象是 。
(3)若A池中原混合液的体积为500 mL,CuSO4、
K2SO4浓度均为0.1 mol/L,电解过程中A池中
共收集到标准状况下的气体 L。
4.6g金属钠与水反应后所得溶液中,要使100个水分子溶有1个钠离子,需要水的质量是( )
A.180g B.181.8g
C.360g D.363.6g
A.180g B.181.8g
C.360g D.363.6g
(1)现有标准状况下的氮气5.6g,其体积为 L,含有氮分子的数目为 。
(2)写出电解食盐水的化学方程式: ;
写出实验室制取氯气的化学方程式: 。
![]()
某天然碱的化学组成可能为aNa2CO3?bNaHCO3?cH2O (a、b、c为正整数),
为确定其组成,化学兴趣小组的同学进行了如下实验:
(1)定性分析:
①取少量天然碱样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝。能否说明样品中含结晶水,试简述理由。
②请你设计一个简单的实验方案,确认样品中含有CO32―离子。
(2)定量分析:该小组同学设计了下图所示装置,测定天然碱的化学组成。
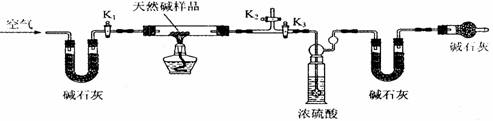
A B C D E
实验步骤:
①按上图(夹持仪器未画出)组装好实验装置后,首先进行的操作是 。
A处碱石灰的作用是 E处碱石灰的作用是
。
②称取天然碱样品7.3g,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶的质量为87.6g,装碱石灰的U型管D的质量为74.7g。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后称得装浓硫酸的洗气瓶质量为88.5g;装碱石灰的U型管D的质量为75.8g。该步骤中缓缓鼓入空气数分钟的目的是
。计算推导:该天然碱的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com