
题目列表(包括答案和解析)
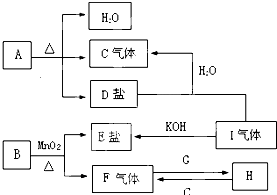 已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答下列问题:
已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答下列问题:
| ||
| ||
| ||
| ||




| ||
| △ |
| ||
| △ |
1.C 2.B 3.B 4.D 5.C 6.B 7.D 8.A 9.C 10.C 11.A
12.D 13.C 14.C 15.C 16.D 17.B 18.B
19.(12分)
(1)CO32- + H2O  HCO3- + OH- (2分)
HCO3- + OH- (2分)
(2)不再有气泡产生(或只有极少量气泡产生)(2分)
(3)玻璃棒(2分)
(4)4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O (2分)
(5)6.6 (2分)
(6)循环使用 (2分)
20.(6分)
(1)Na+[ ]2- Na+ (2分)
]2- Na+ (2分)
(2)C2H6-14e-+18OH- =2CO32-+12H2O (2分)
(3) c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) (2分)
21.(8分)
(1)C + 4HNO3(浓) CO2 ↑ + 4NO2 ↑ + 2H2O (2分,不写条件不得分)
CO2 ↑ + 4NO2 ↑ + 2H2O (2分,不写条件不得分)
SiO32-+CO2 +H2O = H2SiO3↓+CO32 (2分)
(2)8Al+3Fe3O4 9Fe+
9Fe+
Al2O3+2OH-=2AlO2-+H2O (2分)
22.(14分)
(1)增大(2分)
(2)不移动 (2分)
 (3)
(3)
(各占2分,起点位置、曲线走势、终点与原曲线的
相对高低等只要有一处错误则不得分。)
(4)(4分)
0.60(2分)
ν正_>_ν逆(2分)
(5)787.0 (2分)
23:(14分)
(1)羟基;(2分,写结构简式不得分)
 (2)CH2=CH-CH2-OH;(2分)
(2)CH2=CH-CH2-OH;(2分)

 (3)任意1种均可(2分)
(3)任意1种均可(2分)
(4) ① b (2分)
 ②ClCH2COOH,取代反应;(各2分)
②ClCH2COOH,取代反应;(各2分)
③ (2分
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com