
题目列表(包括答案和解析)
下列各选项所述的两个量,前者一定大于后者的是
①3d轨道的能量和4s轨道的能量;②同一电子层中第一个p轨道与第二个p轨道的能量;③2s和3s的轨道半径;④同一原子的基态和激发态;⑤F元素和O元素的电负性;⑥Mg元素和Al元素的第一电离能;⑦H原子和H+离子的半径
A.①⑤⑥⑦ B.②③⑤ C.②④⑦ D.全对
同一原子的基态和激发态相比较
A.基态时的能量比激发态时高 B.基态时比较稳定
C.基态时的能量比激发态时低 D.激发态时比较稳定
3月28日,日本政府宣布从受到破坏的福岛第一核电站区域内土壤中检测出放射性钚-238(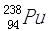 )、钚-239(
)、钚-239( )和钚-240(
)和钚-240( )。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131(
)。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131( )。下列关于钚元素和碘元素的说法正确的是
)。下列关于钚元素和碘元素的说法正确的是
A.钚-238、钚-239和钚-240是同素异形体的关系
B.钚元素和碘元素在元素周期表中都属于主族元素
C.碘-131原子的核外电子数是53,中子数是88
D.基态碘原子的最外层电子排布式是5s25p5
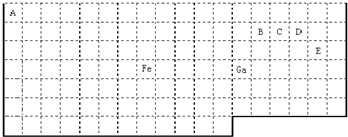
(1)符合上述条件的元素有___________种,原子序数分别是___________。
(2)写出相应元素原子的以下信息 (可填满,也可不填满):
序号 | 元素符号 | 基态原子核外电子排布式 | 在周期表中位置 | 最高正化合价 | 金属元素还是非金属元素 | ||
周期 | 区 | 族 | |||||
元素① |
|
|
|
|
| ||
元素② |
|
|
|
|
| ||
元素③ |
|
|
|
|
| ||
元素④ |
|
|
|
|
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com