
题目列表(包括答案和解析)
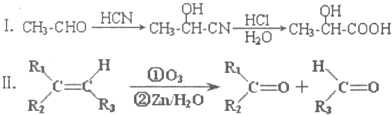
| HCN |
| HCI |
| H2O |
| 浓H2SO4 |
| △ |
| ①O3 |
| ②Zn/H2O |
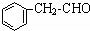
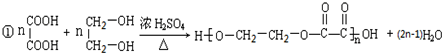


“西气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为1∶1。已知1mol CO气体完全燃烧生成CO2气体放出283kJ热量:1mol氢气完全燃烧生成液态水放出286kJ热量;1mol CH4气体完全燃烧生成CO2气体和液态水放出890kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量 890kJ
(填>、=、<)
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为 ;燃烧生成的CO2的质量比约为 。(最简整数比)
(4)关于用水制取氢气,以下研究方向正确的是 。
A.构成水的氢和氧都是可以燃烧的物质,因此可以研究在不分解水的前提下,使水中的氢成为能源
B.设法聚集太阳光产生高温,使水分解产生氢气
C.寻找高效催化剂,使水较容易分解
D.寻找和制造特殊的化学物质,用于开发廉价能源,以分解水制取氢气
1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的反应热的总和与这个反应一次发生时的反应热相同.”这就是在各反应于相同条件下完成时的有关反应热的重要规律 盖斯定律.已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(固,金刚石)+O2(气)=CO2(气);ΔH=-395.4kJ/mol,C(固,石墨)+O2(气)=CO2(气);ΔH=-393.5kJ/mol.则金刚石转化为石墨时的热化学方程式为________.由此看来更稳定的碳的同素异形体为________.若取金刚石和石墨混合晶体共1mol在O2中完全燃烧,产生热量为Q kJ,则金刚石和石墨的物质的量之比为________(用含Q的式子表示).
盖斯定律.已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(固,金刚石)+O2(气)=CO2(气);ΔH=-395.4kJ/mol,C(固,石墨)+O2(气)=CO2(气);ΔH=-393.5kJ/mol.则金刚石转化为石墨时的热化学方程式为________.由此看来更稳定的碳的同素异形体为________.若取金刚石和石墨混合晶体共1mol在O2中完全燃烧,产生热量为Q kJ,则金刚石和石墨的物质的量之比为________(用含Q的式子表示).
1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律,称为盖斯定律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O2(g)=CO2(g);△H=-395.41kJ/mol,C(石墨、s)+O2(g)=CO2(g);△H=-393.51kJ/mol,则金刚石转化石墨时的热化学方程式为:___________。由此看来更稳定的碳的同素异形体为:____________。若取金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,则金刚石和石墨的物质的量之比为_____________(用含Q的代数式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com