
题目列表(包括答案和解析)
(1)当达到滴定终点时,已知溶液的pH应为9.1左右,现给定甲基橙、酚酞、石蕊三种指示剂,你选择的指示剂是? ?(已知甲基橙、酚酞、石蕊三种指示剂的变色范围分别为3.1~4.4、8.2~10.0、5.0~8.0)。?
(2)某学生的三次实验数据如下:
实验编号 | 取邻苯二甲酸氢钾的质量 | 消耗待测NaOH溶液的体积 |
① |
| (n+0.80)mL |
② |
| g(n+0.10)mL |
③ |
| g(n-0.10)mL |
第一次测定消耗体积较大的原因可能是下列中的 (填序号)。?
①滴定管没有用NaOH溶液润洗,只用了水洗 ②滴定前管尖有气泡,滴定后消失 ③滴定终点把握不准,溶液呈深红色 ④溶液有洒落现象 ⑤滴定终点把握不准,溶液呈粉红色后又马上变为无色 ⑥滴定前俯视读数,滴定后仰视读数?
(3)若m=0.04n,n=17,则c(NaOH)= 。
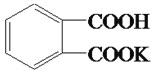 某学生用邻苯二甲酸氢钾(相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1.
某学生用邻苯二甲酸氢钾(相对分子质量为204)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol/L左右,滴定终点时溶液的pH约为9.1.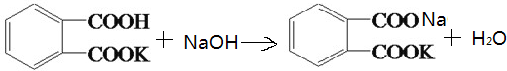
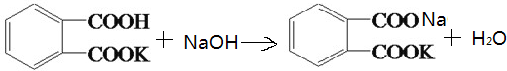
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |
某学生用邻苯二甲酸氢钾 (相对分子质量为204.0)测定NaOH溶液的浓度。若每次都精确取用邻苯二甲酸氢钾为0.2040g,滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该学生进行三次实验,每次消耗氢氧化钠溶液的体积如下表所示:
(相对分子质量为204.0)测定NaOH溶液的浓度。若每次都精确取用邻苯二甲酸氢钾为0.2040g,滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该学生进行三次实验,每次消耗氢氧化钠溶液的体积如下表所示:
(1)NaOH溶液的物质的量浓度为多少?
(2)该学生测定出来的NaOH溶液的物质的量浓度高于其实际值,造成该结果的原因可能是_________。
A.盛放邻苯二甲酸氢钾的锥形瓶未用待装液润洗
B.读取消耗NaOH溶液体积的数值时,滴定前仰视,滴定后俯视
C.滴速太快没来得及观察就已经变色
D.配制NaOH溶液时,NaOH固体中可能混有KOH
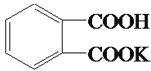
相对分子质量为204.0)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol•L-1左右,滴定终点时溶液的pH约为9.1。该生用托盘天平称量邻苯二甲酸氢钾时,在左盘放有一个1g砝码,游码位置如图所示:
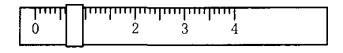
(1)将称好的邻苯二甲酸氢钾放于锥形瓶中,加适量水溶解,溶液无色,再加入指示剂________(从甲基橙、酚酞、石蕊中选择)1~2滴,用NaOH溶液滴定至终点,现象是________。
(2)该生进行三次实验,所取固体质量均相同,填写下表:
实验编号 邻苯二甲酸氢钾质
量/g 待测NaOH溶液体
积/mL
1 18.20
2 17.10
3 16.90
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是(只填三种即可):a________b________c________
(4)NaOH溶液的物质的量浓度为(只列出计算式,不必求出结果)。
1.D 2.C 3.C 4.B 5.D 6.CD 7.B 8.AC 9.A 10.D 11.C 12.AB
13.D 14.D 15.A 16.B 17.B 18.C 19.D 20.B 21.B 22.B
23.(1)A.坩埚 B.蒸发皿 C.分液漏斗 D.蒸馏烧瓶 E.漏斗 F.酒精灯 G.干燥管
(2)①G ②C ③D、F ④E ⑤B、F
24.(1)I (2) ;
; (3)溶解放热,并提供大量的
(3)溶解放热,并提供大量的
(4)①
②
25.分解与解答:(1)电子氧化性 ,而Cu、Fe、Zn全部液解,故一定有
,而Cu、Fe、Zn全部液解,故一定有 、
、 、
、 ,可能还有
,可能还有 、
、
(2)根据氧化还原反应进行的次序规律,因还原性Zn>Fe>Cu,若剩余固体W/ 与Cu反应,
与Cu反应, 与Cu不反应,故一定有
与Cu不反应,故一定有 、
、 ,可能还有
,可能还有 ,一定没有
,一定没有 、
、
(3)剩余固体为Cu、Fe、Zn,只有部分Zn溶解,加之 、
、 均要与Fe反应,故一定有
均要与Fe反应,故一定有 、
、 ,一定没有
,一定没有 、
、 、
、
26.(1)①x=1,y=1;②6、2、4=1、3、2、4;
③
(2) ;Mn
;Mn
27.(1) ;
;
(2) ;
;
(3) ;
;

28.(1)①C ②
(2) ;
; ;在
;在 分子中,C、H质量比为12∶4,在
分子中,C、H质量比为12∶4,在 混入任何比例的
混入任何比例的 都将使C、H质量比小于12∶4;1∶3 25%
都将使C、H质量比小于12∶4;1∶3 25%
(2) 或0.1500 V
%
或0.1500 V
%
(3)C
30.(1)2;5
W、 ;W、
;W、 ;W、
;W、 ;
; 、
、 ;
; 、
、
(2) 或
或 或
或
 www.ks5u.com
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com