
题目列表(包括答案和解析)
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
将0.1 mol/L HCl溶液数滴缓缓滴入1 mol/L 50 mL Na3PO4溶液中,且不断搅拌3H++PO |
B. |
将1 mol/L NaAlO2溶液和1.5 mol/L的HCl溶液等体积互相均匀混合 6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
C. |
向1 mol/L明矾溶液50 mL中滴入数滴0.1 mol/L Ba(OH)2溶液 Al3++2SO |
D. |
将少量SO2气体通入NaClO溶液中:SO2+H2O+ClO-=SO |
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径 /10-10m |
0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52] | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |




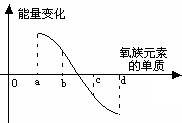
(9分)元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示,
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
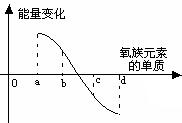
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
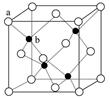
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
| T | 常温常压下,T单质是淡黄色固体,常在火山口附近沉积 |
| P | P的价层电子排布为[Ar]3d104s2 |
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A
A
A
C
B
A
C
BC
D
D
AC
C
CD
AC
D
16.(一)ABDG (二)(1)温度对KIO3稳定性的影响?(或油炸食品是否适宜放碘盐)研究报告、实验报告、论文等.(2)IO3―+5I―+6H+====3I2+3H2O
17. (1)Zn-2e―==Zn2+,2MnO2+H2===Mn2O3+H2O
(3)①向小烧杯中加入一定量的热蒸馏水,充分搅拌,趁热过滤,将滤液冷却,再过滤得晶体,所得晶体即为ZnCl2、NH4Cl;②A.取少许溶液,加NaOH加热,在试管口放湿润红色石蕊试纸;B.试纸变蓝;C.NH4+OH―==NH3+H2O晶体混合物;D.取少许溶液,加……(或氨水),将悬浊液分成两份,一份加稀HCl,一份加足量氨水;E.先白色沉淀,后沉淀都溶解;③加热法;(4)坩埚、玻璃棒(三脚架、泥三角、坩埚钳等)
18.⑴排出装置中的空气(CO2、N2、H2O等);⑵AD,D;
⑶

⑷ 除去过量O2,保证最终收集的气体是反应生成的N2;
⑸水,若是气体,则不能被收集和测量,导致较大误差,充满水时能保证进入装置E的气体体积与排出水的体积基本相当;
⑹①使E、F中的液面相平;②视线与量筒内凹液面最低处相平,
⑺A B D;⑻不能,因为CO2、H2O会被碱石灰同时吸收,使实验结果缺少必要数据
19.⑴同周期从左→右电负性逐渐增大(或同主族……)
⑵2.0<x<2.4,弱;⑶得电子;⑷共价键
20.⑴还原剂;2Fe3++Fe==3Fe2+;⑵重结晶,FeSO4?7H2O;
⑶促进Ti4+完全水解生成沉淀;
| ||||||||||||||