
题目列表(包括答案和解析)
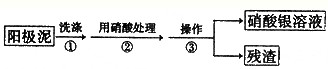
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3 Au(NO3)3+3NO2↑+3H2O Au(NO3)3+3NO2↑+3H2O |
<10-5 |
| 反应2 | Au3++Cl-  [AuCl4]- [AuCl4]- |
>105 |
| ||
| ||
(18分)钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
(1)V2O5是接触法制硫酸的催化剂。 ’
①已知25℃.10lkPa时:
2SO2(g)+O2(g)+2H2O(1)=2H2SO4(1) △H = -457kJ·mol-l
SO3(g)+H2O(1)=H2SO4(1) △H= -130kJ·mol-l 则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
②SO2水溶液可与SeO2反应得到硫酸,当有79gSe生成时,转移电子的物质的量为 mol,此反应的化学方程式是 。
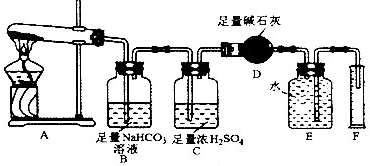
(2)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42-。电池放电时,负极的电极反应为:
V2+-e一=V3+。
①电池放电时的总反应方程式为 。
充电时,电极M应接电源的 极。
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+。则第一步反应过程中阴极区溶液n(H+) (填“增大”、“不变”或“减小”),阳极的电极反应式为: 。
 则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
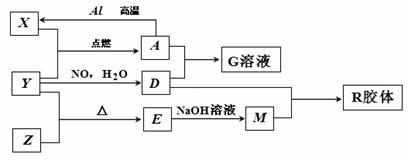
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型为 ;R的化学式是 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
(3)已知A与1molAl反应转化为X时(所有物质均为固体)。放出a kJ热量。写出该反应的热化学方程式: 。
(4)写出A和D的稀溶液反应生成G的离子方程式: 。
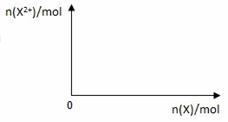 (5)向含4 molD的稀溶液中,逐渐加
(5)向含4 molD的稀溶液中,逐渐加
入X粉末至过量。假设生成的气体只有
一种,请在右面坐标系中画出n(X2+)
随n(X)变化的示意图,并标出n(X2+)
的最大值。


(一)选择题
1.BC2.B3.C.4.C5.C6.C7.B8.C9.BD10.AC11.BD12.D13.B14.C15.D.16.BC17.C18.B19.CD20.CD21.C22.D23.A24.CD25.A26.B27.C28.CD29.B30.A31.C32.(1)D(2)C33.C34.BC35.C36.D37.C38.D39.D40.B、C
(二)非选择题
1.(1)选用AgNO3溶液较好(CuSO4溶液次之,NaCl和H2SO4溶液更次之),①若电解NaCl、H2SO4溶液,产生的气体体积较难测定准确;②同样条件下,通过等量的电量,析出的Ag的质量大于Cu,因而称量和计算时产生的误差前者要小
(2)①电流强度;②电解(通电)时间;③电解产物的质量
(3)NA=
I:电流强度;t:通时间;mAg:析出银的质量MAg:Ag的摩尔质量。
2.(1)BH+2H2O4H2↑+BO―2
(2)pH愈小,反应速率愈大(3)1、16、8、7、4、7
3.DG+CO2M(D)==100D为MCO3,则M(M)=100-60=40M为Ca2+,A为Ca2+盐〔可溶性含氧酸钙盐可能为Ca(NO3)2〕,B为碳酸盐(可溶性碳酸盐有K+、Na+、NH+4……)
从EF+H2O,而F为非金属氧化物,则E含H、O及另一非金属,可推测E为NH4NO3
又:M(F)×+18×M(F)=44,氮的氧化物中N2O相对分子质量为44,和题意相符,可推得A:Ca(NO3)2、B:(NH4)2CO3、D:CaCO3、E:NH4NO3、F:N2O
4.13P4+10P2I4+128H2O32H3PO4+40PH4I
5.5、8、12、10、4、8、12;紫红色溶液褪去;不能用,因为KMnO4与HCl反应,HNO3的氧化性会干扰KMnO4的氧化性。
6.(1)2、5-n、2n、2、5-n、n+3(2)2、+6(3)B、C
7.(1)31.6,36.8,42.1(2)1.58×1024?(3)58.95L/mol(4)42.1g
8.(1)CO;(2)HF;(3)C+H2OCO+H2;(4)2F2+2H2O4HF+O2
9.(1)1cm3中阴、阳离子总数=
1cm3中Ni2+-O2-离子对数=
密度=
(2)设1molNi0.97O中含Ni3+xmol,Ni2+(0.97-x)mol,根据电中性;3xmol+2(0.97-x)mol=2×1mol,x=0.06
Ni2+为(0.97-x)mol=0.91mol
离子数之比Ni3+∶Ni2+=0.06∶0.91=6∶91
10.(1)1∶4;(2)0.12mol;(3)60%
11.(1)1∶50,增大O2量,平衡正向移动,提高SO2转化率(2)保证NH3∶SO2=2∶1(3)3.54t,0.912t.
12.(1)25%(2)2a(3)6(4)n>m
13.(1)BiCl3+H2OBiOCl↓+2HCl(2)不同意,因BiOCl中Cl为-1价而不是+1价。(3)将BiCl3溶解于含适量HCl的蒸馏水中(4)增大溶液中Cl―浓度,抑制BiCl3的水解。
14.(1)NH+Al3++2SO+2Ba2++4OH―2BaSO4↓+Al(OH)3↓+NH3↑+H2O
(2)Al(OH)3+OH―AlO+2H2O
15.(1)HCO+Br2HBrO+Br―+CO2↑
(2)2CO+Br2+H2O2HCO+Br―+BrO―
16.(1)该条件下D的密度ag/L;19.5+11.0-3.00L×ag/L;
(2)盐酸的物质的量浓度bmol/L;当×2≤0.01×b时,盐酸足量:V(H2)=×22.4L
当×2>0.01×b时,盐酸不足:V(H2)=×0.01×b×22.4L。
17.(1)CH3COOHCH3COO―+H+,CH3COO―+H2OCH3COOH+OH―,H2OH++OH―
18.(1)DABF→B→A→C→D→E
(2)2Cl―-2eCl2↑变蓝色Cl2+2I―2Cl―+I2
(3)①③④⑥(4)NA=
19.(1)
(2)N2+O22NO
112
说明氧气过量,过量2体积,根据NO和O2的反应
2NO+O2=2NO
212
说明反应后所得气体NO22体积,O21体积。故密闭容器中气体的体积为3体积。所以
(3)减少,不变。
20.A:NaOHB:NaNO3C:Ba(NO3)2D:HNO3X:MgSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com