
题目列表(包括答案和解析)
下表为元素周期表的一部分,请参照元素A-H在表中的位置,
族 周期 周期 | IA | | 0 | |||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | B | C | D | | |
| 3 | E | | F | G | | | H | |
 (3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。 (4) E、F的最高价氧化物的水化物相互反应的离子方程式
(4) E、F的最高价氧化物的水化物相互反应的离子方程式  。
。 子分别为 和 ,根据等电子理
子分别为 和 ,根据等电子理(8分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:w.w.w.k.s.5.u.c.o.m
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)⑨、⑩的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑥中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中④、⑩两种元素形成的氢化物中沸点高的是 ,说明原因:
(7分)从某物质A的水溶液出发有下图所示的一系列变化: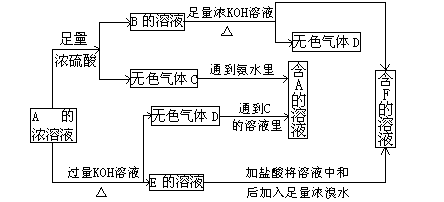
(1)写出下列物质的化学式:w.w.w.k.s.5.u.c.o.m
A 、C 、F 。
(2)写出下列反应的离子方程式
A→E________________________;
E→F________________________。
下列物质的保存方法正确的是 ( )w.w.w.k.s.5.u. c.o.m
①少量金属钠保存在冷水中 ②浓硝酸盛放在无色试剂瓶中
③少量金属钾保存在煤油中 ④氢氧化钠溶液盛放在带有橡胶塞的试剂瓶中
⑤氯水存放在带玻璃塞的无色细口瓶中 ⑥碳酸钠固体保存在带橡胶塞的细口瓶中
A.②③④ B.③④⑥ C.③④ D.①③④
(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
![]()

(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
![]() (2)负极反应式为 。
(2)负极反应式为 。
![]() (3)电极表面镀铂粉的原因为 。
(3)电极表面镀铂粉的原因为 。
![]() (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
![]() Ⅰ.2Li+H2
Ⅰ.2Li+H2![]()
![]() 2LIH
2LIH
![]() Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
![]() ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com