
题目列表(包括答案和解析)
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比
是 .
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与
足量的Ba(OH)2溶液反应的离子方程式 .
(3)在一个装有可移动活塞的容器中进行如下反应:C2(g)+3A2(g)![]() 2CA3(g)
2CA3(g)
ΔH=-92.4 kJ·mol-1.反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2 mol,总容积为1.0 L.
①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是________:
A.C2 0.6mol,A2 0.5mol,CA3 0mol B.C2 0mol,A2 0mol,CA3 1.2mol
C.C2 0.5mol/L,A2 0.3mol/L,CA3 0.2mol/L
②若起始加入1.2molC2、1.0molA2,达平衡后C2的浓度为__________mol/L
③如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将________(填“正向”、“逆向”或“不”)移动.
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比
是 .
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与
足量的Ba(OH)2溶液反应的离子方程式 .
(3)在一个装有可移动活塞的容器中进行如下反应:C2(g)+3A2(g) 2CA3(g)
2CA3(g)
ΔH=-92.4 kJ·mol-1.反应达到平衡后,测得容器中含有C2 0.5mol,A2 0.2mol,CA3 0.2 mol,总容积为1.0 L.
①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是________:
A.C2 0.6mol,A2 0.5mol,CA3 0mol B.C2 0mol,A2 0mol,CA3 1.2mol
C.C2 0.5mol/L,A2 0.3mol/L,CA3 0.2mol/L
②若起始加入1.2molC2、1.0molA2,达平衡后C2的浓度为__________mol/L
③如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将________(填“正向”、“逆向”或“不”)移动.
 7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。
7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。 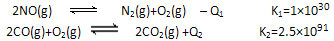
 CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2)
CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2) 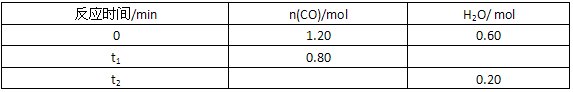


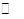 2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: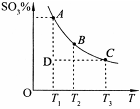
 0(填“>’或“<”)。
0(填“>’或“<”)。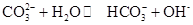 ,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。(16分)向一定体积的密闭器中加入2 mol A、0.6 mo1 C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1 阶段c(B)未画出.图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂.
请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为 。
(2) t4~t5阶段改变的条件为 ,B的起始物质的量浓度为 ,各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
则K1= (保留两位小数),
K1、K2、K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接).
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式
。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .
【解析】(1)化学反应速率通常用单位时间内浓度的变化量来表示。根据图像I可知在15min内C的浓度变化量是0.6mol/L-0.3mol/L=0.3mol/L,所以速率为
(2)由图像Ⅱ可知,在t4~t5阶段反应速率减小,但平衡不移动,所以改变的条件不可能是温度和浓度,由于在t3~t4阶段为使用催化剂,所以该阶段只是降低压强。这说明改变压强平衡不移动,因此反应前后体积是不变的。根据图像I可知A是反应物,C是生成物,二者的变化量之比是2︰3,所以要使反应前后体积不变,B只是反应物,及反应的方程式为2A+B3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为
![]() 。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
(3)根据题意科判断,每消耗0.01molA,反应就吸收能量akJ,所以反应的热化学方程式为2A(g)+B(g)⇋3C(g) △H=+200kJ/mol。
(4)因为容器容积不变(容器容积是2L),所以要使平衡等效,则起始物质的物质的量是相等的。根据题意可知起始时AB的物质的量分别为2.4mol和1.2mol,则把cmol的C转化为AB,则AB的物质的量(mol)分别是a+2c/3、b+c/3,所以关系式必须满足a+2c/3=2.4、b+c/3=1.2.
一.选择题:
题号
1
2
3
4
5
6
7
8
9
10
11
答案
D
B
B
C
B
C
A
D
B
B
C
题号
12
13
14
15
16
17
18
19
20
21
答案
D
B
A
BD
AC
ABC
D
D
AD
BD
22.(共18分)
(1)CD(4分)

23.(16分)解:
⑴ (3分)
(3分)
 (3分)
(3分)
⑵ (4分)
(4分)
 (1分)
(1分)
 (5分)
(5分)
24.(18分)解:
(1) (2分)
(2分)
 (2分)
(2分)
 (2分)
(2分)
射出电场后做匀速直线运动,则在磁场中的速度为2.5×
(2)与速度x轴的夹角
经过电场的偏距 (2分)
(2分)
故有 (2分)
(2分)
(3)作出粒子在磁场中的运动轨迹,如图
则 (3分)
(3分)
因为
解得 (2分)
(2分)
 根据
根据 (3分)
(3分)
25.(20分)解:
(1)前4 s内,金属杆切割磁感线产生的感应电动势为 ①(1分)
①(1分)
由闭合电路欧姆定律可知A的示数 ②(1分)
②(1分)
而由图乙可知 ③(1分)
③(1分)
由②③式得 ④(1分)
④(1分)
由④式可知。随v时间t均匀增大,所以金属杆做匀加速直线运动其中加速度a=
(2)同理,后2 s内
由图乙可知 (其中k‘=
(其中k‘=
由②⑤式得 ⑥(1分)
⑥(1分)
由⑥式可知v‘随时间t‘均匀减小,所以金属杆做匀减速直线运动
其中加速度 (1分)
(1分)
t=5s(即t‘=1s)时,由⑤式得I‘=
安培力 (1分)
(1分)
再由牛顿第二定律有 ⑦(1分)
⑦(1分)
 故
故 (1分)
(1分)
所以F的瞬时功率为P=Fv‘=0.6 W (1分)
(3)前4 s内,由牛顿第二定律有
 (1分)
(1分)
 ⑧(1分)
⑧(1分)
图线为直线, 时,F1=0.55 N,t=4 s时,F2=0.95 N
时,F1=0.55 N,t=4 s时,F2=0.95 N
(1分)
后2 s内,由牛顿第二定律有 (1分)
(1分)
 ⑨(1分)
⑨(1分)
图线为直线, (即t=4 s)时,
(即t=4 s)时, (即t=6 s)时,
(即t=6 s)时, (1分)
(1分)
根据以上分析,作出 图象 见答图 (2分)
图象 见答图 (2分)
26.(14分)(2分×7)
(1)Cu(NO3)2 + 2H2O
 Cu(OH)2
+ 2HNO3
Cu(OH)2
+ 2HNO3
(2)剧烈燃烧,放出大量的热,发出耀眼的白光。
(3)① ③
(4)② 3Fe2+ + NO3-+ 4H+ = 3Fe3+ + NO↑+ 2H2O
④
(5)2Na2O2 + 2Cu(NO3)2 + 2H2O = 2Cu(OH)2+ 4NaNO3 + O2↑
(6)
27. (14分)
(1) B(1分) A (1分) C (1分)
CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O (2分)
(2) ① 2Na + 2CO2  CO
+ Na2CO3 (3分)
CO
+ Na2CO3 (3分)
② 4Na + 3CO2
 2Na2CO3
+ C (3分)
2Na2CO3
+ C (3分)
(3) 将残留物溶于适量水,若有黑色不溶物则证明残留物中有C,在溶液中加足量BaCl2溶液,然后过滤,在滤液中滴加几滴酚酞,若溶液变红,则证明残留物中含有Na2O。 (3分)
28. (16分) (2分×8)
Ⅰ.
A:  或
或  或 C6H5COOCH3
或 C6H5COOCH3
B: 
 或C6H5CH2OCHO
或C6H5CH2OCHO
C: 或
或  或C6H5OCOCH3
或C6H5OCOCH3
D:  或
或  或C6H5CH2COOH
或C6H5CH2COOH
Ⅱ.(1)Br2 NaOH H2O
(2)HOCH2CH2OCH2CH2OCH2CH2OH 40?
(3)
29.(16分)(2分×8)
Ⅰ.(1) 4 5×10-5mol/L (2) 4 1×10-4mol/L
Ⅱ.(1) (2) ① 减小 升温(或通入A气体) ② 任意值 (或C≥0)
(2) ① 减小 升温(或通入A气体) ② 任意值 (或C≥0)
30.(26分)(1)肝 必需氨基酸 (2)a 促甲状腺激素释放激素 肾上腺素 ①②
(3)①电刺激交感神经后引起肾上腺髓质产生的某种物质通过血液循环运送到心脏,促进心跳加快。
②第二步:电刺激甲鼠支配肾上腺髓质的交感神经,立即用等渗溶液提取甲鼠肾上腺髓质组织液。
第三步:将提取液注射到乙鼠体内。一段时间后测定乙鼠的心率并记录。
Ⅱ.(1)A DEF 。 m/125 千焦 。D增多,F减少 。
(2) 兔→狼 草 兔
|