
题目列表(包括答案和解析)
A、B、C、D、E、F六种强电解质,它们在水中电离出的离子如右表所示,
阳离子 | Cu2+、K+、Fe2+、H+ |
阴离子 | SO42— 、OH- 、NO3- |
其中A、D、F电离产生的阳离子均为K+。另有甲、乙、丙三种固体,它们分别是铁粉、铜粉和Cu(OH)2固体中的某一种,它们与A、B、C、D、E在常温下有如下转化关系:
①固体乙+B溶液→E溶液+氢气
②固体甲+B溶液→C溶液+水
③A溶液+C溶液→固体甲+D溶液
请回答下列问题:
(1)写出下列物质的化学式:甲 ,乙 ,F 。
(2)写出下列反应的离子方程式:
反应① ;
反应③ 。
(3)用题目所涉及到的物质表示丙→C的化学方程式____________________
某种碱式碳酸铜其组成可表示为 ,在加热的条件下,反应为
,在加热的条件下,反应为
 2CuO+
2CuO+ ↑+(x+1)
↑+(x+1) ,某同学粗略取一定样品,先后进行两个实验:实验(Ⅰ):测定
,某同学粗略取一定样品,先后进行两个实验:实验(Ⅰ):测定 中x的值.实验
中x的值.实验
(Ⅱ)用实验(Ⅰ)中所得固体与氢气反应.
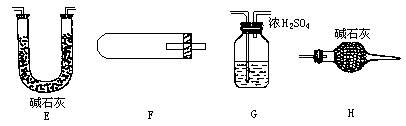
(1)现已装置好如下图所示的实验装置甲、乙,装置中一些附加设置均已略去,其中________是用来完成上述实验________的(填标号).为安全起见,本实验开始后应在你选用的装置的B处________.

(2)用下图中的仪器(必要的铁架台、铁夹、酒精灯均在图中略去)组装一个实验装置,完成另一个实验.组装时,仪器按气流方向从左到右连接顺序为________→________→________→________,这套装置中,H的作用是什么________.
(3)为测定和计算碱式碳酸铜粉末中的x值,某个细心的同学在实验前后准确称量了一些仪器的质量(连同所盛试剂)分别记为 (F装置连同药品反应前后的质量差,取正值,下同)、
(F装置连同药品反应前后的质量差,取正值,下同)、 ,为求x,这几个数据可用的是________,它们的组合有________种.
,为求x,这几个数据可用的是________,它们的组合有________种.
化学方程式练习
一、用化学方程式表示下列各种物质的实验室制法
1、O2(三种方法):
2、H2:
3、Cl2:
4、NH3:
5、CO2:
6、NO:
二、用方程式表示工业生产过程(参考选修Ⅱ,带*的写离子方程式,注意反应条件)
1、氯碱工业(电解饱和食盐水)
*阳极:
*阴极:
*总反应:
2、接触法制硫酸(硫铁矿为原料)
①沸腾炉: ;其中氧化产物为:
②接触室: ;
V2O5的作用是 ,反应温度控制在400~500℃的原因是
③吸收塔:
用98%H2SO4吸收SO3而不用水直接吸收的原因是
。
④尾气处理:
3、海水提溴:
*①氯化:
②吹出
③吸收:
④转化:
4、合成氨:
①由水和碳合成H2
②合成塔:
5、氨氧化制硝酸
①氧化炉:
②吸收塔:
③制取化肥硝酸铵:
6、冶炼铝(冰晶石作熔剂)
①碱溶:
②沉淀:
③脱水:
④电解:*阳极:
*阴极:
总反应:
7、铝热法制铁
8、由三氧化钨制钨
9、工业制漂白粉
10、制玻璃
11、工业生产石灰浆
12、联合制碱法:
13、高纯硅的生产
。
14、炼铁炼钢
①还原剂的生成:
;
②铁的还原(将铁的氧化物,如Fe2O3还原):
③将生铁脱硫去磷降低含碳量即得钢。
三、完成下列反应的化学方程式(注意写反应条件)。
1、Fe + H2O(g)=
2、C+ H2O(g) =
3、CO+ H2O(g) =
4、F2+ H2O=
5、NH3+H2O
6、NO2+ H2O=
7、SO2+ H2O
8、Cl2 + H2O=
9、K + H2O=
10、Na2O2+ H2O=
11、CaC2+ H2O=
12、Mg3N2+ H2O =
13、Al + NaOH+ H2O=
14、CaCO3+ H2O+ CO2=
15、Fe(OH)2+ H2O+ O2=
16、FeCl3+ H2O
17、NH4Cl+H2O
18、Na2CO3+H2O
19、CuSO4+H2O电解
20、Na2S2O3 + HCl =
21、SiO2 + HF=
22、SiO2 + NaOH=
23、Na2SiO3+ HCl=
四、写出下列物质分别与NaOH溶液反应的化学方程式。
1、Si
2、Cl2
3、SiO2
4、SO2 (足量)
5、CO2(小量)
6、H3PO4
7、H2SO4
8、CH3Br
9、Al
10、Al2O3
11、AlCl3
12、Al(OH)3
13、CuSO4
14、NaHCO3
15、Ca(HCO3)2(足量)
16、(NH4)2SO4
五、写出下列物质受热或光照的化学方程式。
1、NaHCO3
2、HNO3
3、AgBr
4、H2SO3
5、NH4HCO3
6、Cu(OH)2
7、Ca(HCO3)2
8、Cu2(OH)2CO3
9、H2O2
10、KClO3
11、KMnO4
12、NH4Cl
13、HClO
14、CH4+Cl2
15、H2+Cl2
16、CuO
六、写出下列反应的化学方程式和离子方程式
1、SO2使溴水褪色:
2、SO2使酸性高锰酸钾溶液褪色:
3、氢氧化铁溶于氢碘酸:
4、乙二酸(草酸)使酸性高锰酸钾溶液褪色 :
5、用石灰水与小苏打溶液制烧碱:
6、硫酸氢铵与氢氧化钡溶液混合:
7、漂白粉溶液中充入足量CO2:
8、KHSO4与氢氧化钡溶液混合呈中性:
9、Fe3O4溶于稀硝酸:
10、明矾溶液中加Ba(OH)2溶液至沉淀量最大:
七、用离子方程式表示下列在溶液中的反应
1、KCl+AgNO3:
2、Ba(OH)2+H2SO4:
3、BaCO3+HCl:
4、Cu(OH)2+HCl:
5、Fe(OH)2+HNO3(稀) :
6、FeCl3+KSCN:
7、FeBr2+Cl2(物质的量之比为1:1):
8、NaBr+Cl2:
9、Fe+CuCl2:
10、Zn+AgNO3:
11、纯碱水解:
12、明矾净水:
13、铜和稀硝酸:
14、配制银氨溶液:
15、Na2O2投入稀硫酸中:
八、写出下列物质在空气中变质的化学方程式
1、Na2SO3:
2、NaOH:
3、NO:
4、Na:
5、Na2O2:
6、铜生锈:
7、氯水:
8、白磷:
9、稀硫酸酸化的FeSO4溶液变棕黄色
10、无色KI溶液变棕黄色
11、漂白粉失效:
九、写出下列反应的化学方程式
1、混合H2S和SO2生成硫和水:
2、炭加热放入浓硫酸中:
3、乙醇催化氧化为乙醛:
4、乙醛与银氨溶液反应:
5、乙醛与新制Cu(OH)2加热:
6、铜与浓硫酸共热:
7、氧化硫通入浓溴水:
8、铜与浓硝酸反应:
9、木炭和浓硝酸共热:
10、FeCl3溶液中加入KI溶液:
11、高锰酸钾固体中滴入浓盐酸:
12、氨水通入少量SO2:
13、偏铝酸钠溶液中加足量稀硫酸:
14、NaAlO2溶液中充入足量CO2:
15、Ba(AlO2)2溶液中加入硫酸铝溶液:
16、氢氧化亚铁水溶液在空气中变质:
12、氯化铁溶液溶解铜:
十、按要求写方程式
1、写出高温条件下发生的置换反应四个:
①
②
③
④
2、写出一个点燃条件下的置换反应:
3、写出一个加热条件下的置换反应:
4、写出一个有三种反应物的置换反应:
5、写出工业生产中需要高温条件的反应(不少于5个)的化学方程式:
6、试设计一个实验,检验某溶液中存在Fe2+,请在下面的横线上按操作顺序写出相应的离子方程式: 。
7、治疗胃酸过多的药物中常用Al(OH)3,如何用氧化铝制取氢氧化铝?要求制取过程中酸碱的用量降到最少。按生产顺序写出相关的离子方程式: 。
8、化学反应中有的具有相似性,有的反应具有特殊性,试写出下列相关化学方程式,并思考其中的原因:
① Li + O2
Na + O2
② Mg + CO2
Mg + SO2
③ Na2O2 + CO2
Na2O2 + SO2
KO2 + CO2
④ F2 + H2O
Cl2 + H2O
⑤ Fe + Cl2
Fe + I2
⑥ Fe(OH)3 + HCl
Fe(OH)3 + HI
9、按要求写化学方程式
①碱性氧化物与水反应(举2例)
②碱性氧化物与酸反应(举2例)
③金属氧化物但不是碱性氧化物的氧化物与水反应(举一例)
④酸性氧化物与水反应(举2例,其中一例为金属氧化物)
⑤能与水反应生成酸,但不是酸性氧化物也不是碱性氧化物氧化物与水反应的化学方程式:
。
⑥列举不少于5类既能与强酸反应,又能与强碱反应的物质,并分别写出它们与酸(HCl)、碱(NaOH)反应的离子方程式:
A、物质化学式:
B、物质化学式:
C、物质化学式:
D、物质化学式:
E、物质化学式:
F、物质化学式:
G、物质化学式:
10、某酸性氧化物,它能与某些酸反应,也能与碱反应,请写出这样的氧化物一种,并写出它与酸反应的化学方程式和与碱反应的离子方程式:
氧化物分子式:
1.B 解析:观察细胞质流动时不需要对叶片进行染色。
2.C 解析:从实验可以看出:若 ,说明光不会使向光侧的生长素分解;若
,说明光不会使向光侧的生长素分解;若 ,则光使向光侧的生长素分解;若
,则光使向光侧的生长素分解;若 ,则不符合题意。任何条件下都是
,则不符合题意。任何条件下都是 ,否则不符合题意。若
,否则不符合题意。若 ,说明光使向光侧的生长素分解;若
,说明光使向光侧的生长素分解;若 ,且
,且 ,则光使向光侧的生长素分解,同时光使生长素向背光侧运输;若
,则光使向光侧的生长素分解,同时光使生长素向背光侧运输;若 ,且
,且 ,则光使生长素向背光侧运输。
,则光使生长素向背光侧运输。
3.B
4.D解析:在用酵母菌生产酒的过程中,处于生长期的酵母菌进行的是有氧呼吸,所以不能以酒精浓度测定其生长状况。
5.C解析:基因治疗是把健康的外源基因导入有基因缺陷的细胞中从而达对治疗疾病的目的;紫草素是从愈伤组织中提取的;叶绿体DNA上的基因控制的遗传是细胞质遗传(即母系遗传),所以④的做法是可以防止基因污染的;植物体细胞杂交技术可以克服远源杂交不亲和障碍,扩大了用于杂交的亲本组合范围。
6.C 7.C 8.D 9.B 10.C 11.A 12.C 13.D 14.AC 15.B 16.BD 17.A 18.D 19.B 20.CD 21.B
22.Ⅰ (1分) 不改变 (1分) 无关 (2分)
(1分) 不改变 (1分) 无关 (2分)
加速度与倾角的正弦值成正比(2分)
如图所示(2分)
 |
Ⅱ.(1)电路图和实物图分别如图甲、乙所示(每图3分)
 |
(2)D (2分) (3)D(2分)
23.解:(1)小球从上圆环顶部释放,根据自由落体运动规律有: (3分)
(3分)
解得小球到达地面所用的时间 . (2分)
. (2分)
(2)设轨道 与水平面间的夹角为
与水平面间的夹角为 ,如图所示,由几何关系可知:
,如图所示,由几何关系可知:
 轨道
轨道 的长度
的长度 (3分)
(3分)
由牛顿第二定律可知,小球下滑的加
速度 (2分)
(2分)
由运动学公式可得: (2分)
(2分)
联立解得: . (2分)
. (2分)
24.解:(1)A球在电场力作用下做初速度为零的匀加速直线运动,设加速度的大小为 ,经过时间
,经过时间 与B球发生碰撞,则有:
与B球发生碰撞,则有:
 (2分)
(2分)  (2分)
(2分)
解得: (2分)
(2分)
(2)设A球与B球发生碰撞前的速度为 ,碰撞后A球的速度为
,碰撞后A球的速度为 ,B球的速度为
,B球的速度为 ,则有:
,则有: (1分)
(1分)
A、B两球碰撞过程中动量守恒,则有: (2分)
(2分)
根据题意,有: (2分)
(2分)
联立解得: (1分),
(1分), (1分)
(1分)
A球与B球发生碰撞后,B球做平抛运动;A球在竖直方向上做自由落体运动,在水平方向上做初速度为零的匀加速运动.A球与B球落地前的运动时间相等,并设运动时间为 ,在这段时间内A、B两球在水平方向上发生的位移分别为
,在这段时间内A、B两球在水平方向上发生的位移分别为 和
和 ,则有:
,则有:
 (1分) 解得:
(1分) 解得: (1分)
(1分)
故 (1分),
(1分), (1分)
(1分)
A、B落地点之间的距离 .(1分)
.(1分)
25.解:(1)粒子在Ⅰ、Ⅲ区域内运动时,有: (2分)
(2分)

 (1分) 解得:
(1分) 解得: (2分)
(2分)
粒子在Ⅱ区域内运动时满足: (2分)
(2分)
解得: ,方向水平向右(2分)
,方向水平向右(2分)
同理可得: ,方向水平向左. (2分)
,方向水平向左. (2分)
(2)粒子的运动轨迹如图所示,根据对称性,在区域Ⅲ中
只能存在匀强磁场,且满足:  ,方向垂直纸面向外(2分)
,方向垂直纸面向外(2分)
由于周期相等,可以在区域Ⅱ内 轴左侧加匀强电场,方向平行于
轴左侧加匀强电场,方向平行于 轴,使粒子沿
轴,使粒子沿 轴方向的速度保持不变,从B点到
轴方向的速度保持不变,从B点到 点做类平抛运动,时间
点做类平抛运动,时间 (2分)
(2分)
粒子沿 轴方向的位移是
轴方向的位移是 ,有:
,有: (2分)
(2分)
由牛顿第二定律,有: (1分)
(1分)
代人数据解得: ,方向平行于
,方向平行于 轴向右(2分)
轴向右(2分)
根据对称性,区域Ⅱ内 轴右侧加匀强电场,场强大小
轴右侧加匀强电场,场强大小 ,方向平行于
,方向平行于 轴向左.(2分)
轴向左.(2分)
26.(1)  (2分) (2)
(2分) (2)  (3分)
(3分)
(3) 

 (3分)
(3分)
(4)  ;
; (3分) (5)
(3分) (5)  (3分)
(3分)
27.(1)  ;
; ;
; ;
; (各2分)
(各2分)
(2) 
 (各3分)
(各3分)
28.(1)  (2分)
(2分)
(2)  ;将盛放药品的试管口向上倾斜并改用向上排空气法收集气体(各2分)
;将盛放药品的试管口向上倾斜并改用向上排空气法收集气体(各2分)
(3)  (2分) (4)
(2分) (4)  (2分);
(2分);
方案序号
分析
误差(填“偏高”或“偏低”)
A
碱石灰除吸收 外,还吸收
外,还吸收 ,测得
,测得 的质量增大(1分)
的质量增大(1分)
偏低(1分)
B
 在空气中烘干称量过程中部分被氧化生成
在空气中烘干称量过程中部分被氧化生成 ,固体的质量增大(1分)
,固体的质量增大(1分)
偏低(1分)
(5)反应结束后将烧瓶中的铜片取出,洗涤、干燥后称量,根据反应的铜片计算反应的硫酸,再计算剩余硫酸溶液的浓度。(其他答案合理也可) (3分)
 |
29.(1)取代; (各2分) (2)
(其他合理答案也可)(2分)
(各2分) (2)
(其他合理答案也可)(2分)

(3)
(3分)
 (4)
(4) (3分)
(3分)
(5) (3分)
30.Ⅰ.(1)都是 首先被固定为
首先被固定为 在维管束的外面,没有两圈花环型的细胞
在维管束的外面,没有两圈花环型的细胞
(2)晚上无光照,光反应不能正常进行,无法为暗反应提供所需的ATP、NADPH
有氧呼吸(呼吸作用) 线粒体
(3)  有利于降低植物的蒸腾作用,减少植物体内水分的散失
有利于降低植物的蒸腾作用,减少植物体内水分的散失
(4)干旱地区
(5)气孔关闭,限制了植物对 的吸收,影响了暗反应的正常进行(每空2分,计18分)
的吸收,影响了暗反应的正常进行(每空2分,计18分)
Ⅱ.(1)微生物的氧化分解 化石燃料的燃烧 ③④⑦
(2)非生物的物质(或大气中的二氧化碳库)
(3)  群落中各生物成分的呼吸量(或生产者、消费者和分解者的呼吸量)
群落中各生物成分的呼吸量(或生产者、消费者和分解者的呼吸量) 
(4)能量流动 (每空1分,计8分)
31.(1)  长 (2)
长 (2) 

(3)直毛和分叉毛 常染色体
(4)第二步:残翅分叉毛雌 第三步:后代表现型的种类和比例 预期结果:雌蝇中长翅直毛:残翅直毛= ,雄蝇中长翅分叉毛:残翅分叉毛=
,雄蝇中长翅分叉毛:残翅分叉毛= (或长翅直毛雌:残翅直毛雌:长翅分叉毛雄:残翅分叉毛雄=
(或长翅直毛雌:残翅直毛雌:长翅分叉毛雄:残翅分叉毛雄= )(每空2分,计16分)
)(每空2分,计16分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com