
题目列表(包括答案和解析)
 I3-,故标准I2溶液应配成I2的KI溶液)进行滴定,原理如下:
I3-,故标准I2溶液应配成I2的KI溶液)进行滴定,原理如下: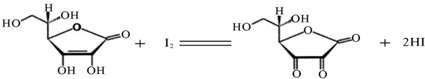

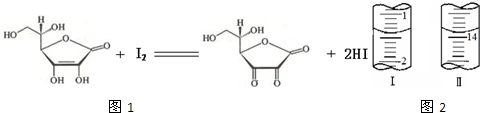
(10分)维生素C(C6H8O6,相对分子质量为176)可溶于水,具有强还原性,在碱性溶液中易被空气氧化,在酸性介质中较为稳定。维生素C通常用标准I2溶液(I2在水中溶解度很小,易溶于KI溶液,I2+I–![]() I3–,故标准I2溶液应配成I2的KI溶液)进行滴,原理如下:
I3–,故标准I2溶液应配成I2的KI溶液)进行滴,原理如下:

(1)滴定过程中应选用 (填酸式或碱式)滴定管盛放标准I2溶液,滴定所用的指示剂为 ,出现 现象时即为滴定终点。
(2)待测维生素C溶液在配制过程中,可以加入下列试剂中的 (填字母)
 A.0.1 mol·L-1 CH3COOH B.0.1 mol·L-1 HNO3
A.0.1 mol·L-1 CH3COOH B.0.1 mol·L-1 HNO3
C.0.1 mol·L-1 NaOH D.0.1 mol·L-1 Na2SO3
(3)配制一定物质的量浓度的标准I2溶液所需玻璃仪器有 (填字母)
A.容量瓶 B.胶头滴管 C.玻璃棒 D.烧杯 E.量筒
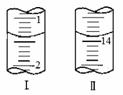
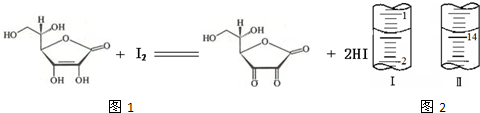
(4)将1.0 g 维生素样品制成100 mL溶液,取25 mL用0.1 mol·L-1的I2溶液滴定,滴定前后滴定管中示数如图,则样品中维生素C的质量分数为 。
 I3-,故标准I2溶液应配成I2的KI溶液)进行滴定,原理如下:
I3-,故标准I2溶液应配成I2的KI溶液)进行滴定,原理如下:

说明:1. 文字简答题以关键词到位为准,按点给分;
2. 化学用语书写:(1)方程式未配平不得分、无条件扣一半分值;
(2)化学式书写错误得0分;
3. 写名称或化学式正确的正常给分; 4. 其他合理解法正常给分。
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意。)
二、选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
A
C
B
D
A
B
D
B
AC
C
A
BD
D
AD
第Ⅱ卷(非选择题 共72分)
三、(本题包括1小题,共10分)
15.(10分)(1)NH4[CuCl2] =CuCl↓+NH4Cl(1分),避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分(1分)。(2)蒸馏(1分),NH4Cl、HNO3(2分)。 (3) B(2分) (4)氯化铵溶于水吸收大量热量,造成反应液温度降低(1分)。 烧瓶上方红棕色气体逐渐变为无色(1分),a或c(1分)(答a或答c给分)
四、(本题包括2小题,共18分)
16.(8分)(1)六 ⅣA (各1分,共2分)(2)不变(2分)
(3) Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O (2分)
(4)Na2S2O3标准溶液浓度和滴定溶液体积(2分)
17.(10分)(1)CH4+H2O
 CO+3H2(2分)(2)n (2分)(3)Fe2O3?H2O(2分)
CO+3H2(2分)(2)n (2分)(3)Fe2O3?H2O(2分)
 |
(4) 优点是:NaOH可以循环利用,同时获得副产品氢气。(各2分,共4分,优点答到“NaOH可以循环利用”即可)
五、(本题包括1小题,共10分)
18.(10分)(1)氯化铵(2分)
(2)原因是降低KH2PO4溶解度,使其析出后,降低了生成物浓度,(同时生成的HCl与三正丁胺反应,也降低了HCl的浓度),使平衡向正反应方向移动。(2分,答到一点即可)。分离出氯化氢(2分,其他合理答案均给分)(3)50―60均可,95%(填近似值即可)(各2分,共4分)
六、(本题包括1小题,共12分)
19.(12分)(1)与生成的硫酸反应,促进平衡向正反应方向移动。(2分)
(2) (2分)
(2分)
(3)2(1分)
(4) (2分)
(2分)
(5)保护A中的酚羟基。(2分)
(6)(3分,第一步正确得2分,完全正确得3分)

|