
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
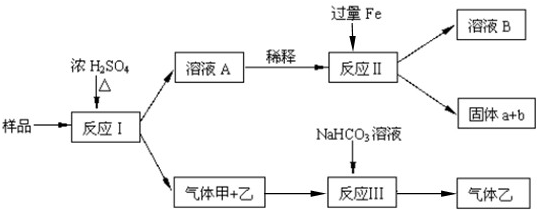
£®12∑÷£©”…Fe2O3°¢Fe°¢CuO°¢C°¢Al÷–µƒº∏÷÷ŒÔ÷ ◊È≥…µƒªÏ∫œ∑€ƒ©£¨»°—˘Ω¯––œ¬¡– µ—È(≤ø∑÷≤˙ŒÔ¬‘»•)£∫
![]()

![]() (1)»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
(1)»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
![]() (2)ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
(2)ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
![]() ¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯Ãµƒ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «______________________________°£
¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯Ãµƒ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «______________________________°£
![]() ¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øµƒÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «________________°£
¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øµƒÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «________________°£
![]() (3)œÚY÷–Õ®»Îπ˝¡øµƒCl2£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «(ÃÓ–¥¿Î◊”∑˚∫≈)________________°£
(3)œÚY÷–Õ®»Îπ˝¡øµƒCl2£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «(ÃÓ–¥¿Î◊”∑˚∫≈)________________°£
![]() (4)»°Y÷–µƒ»Ð“∫£¨µ˜Ω⁄pH‘ºŒ™7£¨º”»ÎµÌ∑€KI∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2molI£≠ ±£¨π≤◊™“∆3molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_________________________________°£
(4)»°Y÷–µƒ»Ð“∫£¨µ˜Ω⁄pH‘ºŒ™7£¨º”»ÎµÌ∑€KI∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2molI£≠ ±£¨π≤◊™“∆3molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_________________________________°£
![]() (5)¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶£¨»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «(∏˜◊È∫œ÷–ŒÔ÷ ”√ªØ—ß Ω±Ì æ)__________________________°£
(5)¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶£¨»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «(∏˜◊È∫œ÷–ŒÔ÷ ”√ªØ—ß Ω±Ì æ)__________________________°£
£®12∑÷£©”…Fe2O3°¢Fe°¢CuO°¢C°¢Al÷–µƒº∏÷÷ŒÔ÷ ◊È≥…µƒªÏ∫œ∑€ƒ©£¨»°—˘Ω¯––œ¬¡– µ—È(≤ø∑÷≤˙ŒÔ¬‘»•)£∫
![]()

![]() (1)»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
(1)»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
![]() (2)ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
(2)ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
![]() ¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯Ãµƒ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «______________________________°£
¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯Ãµƒ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «______________________________°£
¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øµƒÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «________________
(3)œÚY÷–Õ®»Îπ˝¡øµƒCl2£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «(ÃÓ–¥¿Î◊”∑˚∫≈)________________°£
(4)»°Y÷–µƒ»Ð“∫£¨µ˜Ω⁄pH‘ºŒ™7£¨º”»ÎµÌ∑€KI∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2molI£≠ ±£¨π≤◊™“∆3molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_________________________________°£
(5)¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶£¨»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «(∏˜◊È∫œ÷–ŒÔ÷ ”√ªØ—ß Ω±Ì æ)__________________________°£

(1)»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «£®ÃÓ–¥ªØ—ß Ω£©______________°£
(2)ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶I÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯ÃµƒªØ—ß∑Ω≥Ã Ω «_______________________________________________________°£
¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «_________________°£
(3)œÚY÷–Õ®»Îπ˝¡ø¬»∆¯£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «£®ÃÓ–¥¿Î◊”∑˚∫≈£©___________________________°£
(4)»°Y÷–µƒ»Ð“∫£¨µ˜pH‘ºŒ™7£¨º”»ÎµÌ∑€KI»Ð“∫∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2 mol I- ±£¨π≤◊™“∆3 molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_________________________°£
(5)¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶°£»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «£®∏˜◊È∫œ÷–µƒŒÔ÷ ”√ªØ—ß Ω±Ì æ£©____________________________________°£
”…Fe2O3°¢Fe°¢CuO°¢C°¢Al÷–µƒº∏÷÷ŒÔ÷ ◊È≥…µƒªÏ∫œ∑€ƒ©£¨»°—˘Ω¯––œ¬¡– µ—È(≤ø∑÷≤˙ŒÔ¬‘»•)£∫
![]()

![]() £®1£©»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
£®1£©»°…Ÿ¡ø»Ð“∫X£¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨”–≥¡µÌ…˙≥…°£»°…œ≤„«Â“∫£¨Õ®»ÎCO2£¨ŒÞ√˜œ‘±‰ªØ£¨Àµ√˜—˘∆∑÷–≤ª∫¨”–µƒŒÔ÷ «(Ãѧ Ω)________________°£
![]() £®2£©ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
£®2£©ZŒ™“ª÷÷ªÚ¡Ω÷÷∆¯Ã£∫
![]() ¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯ÃµƒªØ—ß∑Ω≥Ã Ω «_____________________________°£
¢Ÿ»ÙZ÷ªŒ™“ª÷÷∆¯Ã£¨ ‘º¡aŒ™±•∫ÕNaHCO3»Ð“∫£¨‘Ú∑¥”¶¢Ò÷–ƒÐÕ¨ ±…˙≥…¡Ω÷÷∆¯ÃµƒªØ—ß∑Ω≥Ã Ω «_____________________________°£
![]() ¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øµƒÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «______°£
¢⁄»ÙZŒ™¡Ω÷÷∆¯ÃµƒªÏ∫œŒÔ£¨ ‘º¡aŒ™ ¡øµƒÀÆ£¨‘ÚZ÷–¡Ω÷÷∆¯ÃµƒªØ—ß Ω «______°£
![]() £®3£©œÚY÷–Õ®»Îπ˝¡øµƒCl2£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «(ÃÓ–¥¿Î◊”∑˚∫≈)________________°£
£®3£©œÚY÷–Õ®»Îπ˝¡øµƒCl2£¨≤¢≤ª∂œΩ¡∞Ë£¨≥‰∑÷∑¥”¶∫Û£¨»Ð“∫÷–µƒ—Ù¿Î◊” «(ÃÓ–¥¿Î◊”∑˚∫≈)________________°£
![]() £®4£©»°Y÷–µƒ»Ð“∫£¨µ˜Ω⁄pH‘ºŒ™7£¨º”»ÎµÌ∑€KI∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2molI£≠ ±£¨π≤◊™“∆3molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_______________°£
£®4£©»°Y÷–µƒ»Ð“∫£¨µ˜Ω⁄pH‘ºŒ™7£¨º”»ÎµÌ∑€KI∫ÕH2O2£¨»Ð“∫≥ ¿∂…´≤¢”–∫Ï∫÷…´≥¡µÌ…˙≥…°£µ±œ˚∫ƒ2molI£≠ ±£¨π≤◊™“∆3molµÁ◊”£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «_______________°£
![]() £®5£©¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶£¨»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «(∏˜◊È∫œ÷–ŒÔ÷ ”√ªØ—ß Ω±Ì æ)_________________°£
£®5£©¡Ì»°‘≠—˘∆∑£¨º”»Î◊„¡øœ°¡ÚÀ·≥‰∑÷∑¥”¶£¨»Ù»Ð“∫÷–“ª∂®≤ªª·≤˙…˙Y÷–µƒ∫Ï…´πÃ㨑ڑ≠—˘∆∑÷–À˘”–ø…ƒÐ¥Ê‘⁄µƒŒÔ÷ ◊È∫œ «(∏˜◊È∫œ÷–ŒÔ÷ ”√ªØ—ß Ω±Ì æ)_________________°£
1
2
3
4
5
6
7
8
C
D
D
D
C
B
B
D
9
10
11
12
13
14
D
BC
BC
B
AB
CD
15£Æ£®10∑÷£© £®1£©¢Ÿ ∑˙¿Î◊” Ω·ππ æ“‚Õº £®1∑÷£©
¢⁄ »°–Œ◊¥¥Û–°œýÕ¨µƒ√æ∆¨∫Õ¬¡∆¨∑÷±”Îê˝œýÕ¨°¢≈®∂»œýÕ¨µƒœ°—ŒÀ·∑¥”¶£¨π€≤Ï≤˙…˙∆¯≈ðµƒøϬ˝ £®2∑÷£©£®≤Ÿ◊˜1∑÷£¨π€≤Ï÷∏±Í1∑÷°£◊≈÷ÿ∫≈≤ø∑÷»±“ª¥¶ø€1∑÷°£”√Ω Ù”Î∑–ÀÆ∑¥”¶°¢µ»≈®∂»—Œ»Ð“∫ºÓ–‘±»Ωœµ»∫œ¿Ì∑Ω∑®æ˘µ√∑÷£¨∑Ω∞∏ŒÞø…–––‘≤ª∏¯∑÷°££©
¢€ Na2SO3 + SO2 + H2O £Ω 2NaHSO3 £®2∑÷£©£®ªØ—ß Ω¥Ìµ√0∑÷£¨≈‰∆Ω¥Ìø€1∑÷£©
”–∞◊…´Ω∫◊¥≥¡µÌ…˙≥…£¨”–ŒÞ…´¥Ãº§–‘∆¯Œ∂∆¯ÃÂ≤˙…˙ £®2∑÷£©
£®∏˜’º1∑÷£¨◊≈÷ÿ∫≈≤ø∑÷”–»±¬©∫œø€1∑÷£©
£®2£©¢Ÿ H2PO4£≠°¢HCO3£≠°¢HPO42£≠ £®2∑÷£© ¢⁄ «ø £®1∑÷£©
16£Æ£®11∑÷£©£®1£©≥˝»•±Ì√ʵƒ”ÕŒ€ CO32£≠ + H2O  HCO3£≠ + OH£≠ £®2∑÷£©
HCO3£≠ + OH£≠ £®2∑÷£©
£®2£©≤ª‘Ÿ”–∆¯≈ð≤˙…˙£®ªÚ÷ª”–º´…Ÿ¡ø∆¯≈ð≤˙…˙£© £®1∑÷£©
£®3£©»Ùøÿ÷∆≤ª◊º»∑Œ¬∂»π˝∏þFe2+“◊±ª—ıªØ£ª”…”⁄”–«‚∆¯…˙≥…£¨√˜ªº”»»≤ª∞≤»´
£®¡Ω∏ˆ∑Ω√Ê∏˜’º1∑÷£©
£®4£©4Fe2+ + O2 + 4H+ £Ω 4Fe3+ + 2H2O £®2∑÷£© £®ªØ—ß Ω¥Ìµ√0∑÷£¨≈‰∆Ω¥Ìø€1∑÷£©
£®5£©6.6 £®2∑÷£©°°°°£®∂ý–¥µ•Œªg≤ªø€∑÷£©
£®6£©—≠ª∑ π”√ £®2∑÷£®æþÃÂÀµ≥ˆ»Á∫Œ—≠ª∑ π”√Õ¨—˘µ√∑÷£¨“‚ÀºœýΩ¸±Ì¥Ô«∑«ÂŒ˙ø€1∑÷£©
17£Æ£®11∑÷£©
£®1£©2MnO4£≠ +
5H
£®ªØ—ß Ω¥Ìµ√0∑÷£¨≈‰∆Ω¥Ìø€1∑÷£¨¬©°¸ø€1∑÷£¨ø€ÕÍŒ™÷π£©
£®2£©4 £®2∑÷£©
£®3£©¢Ÿ ∑¥”¶ø™ º ±£∫c(KMnO4)£Ω £Ω0.00067 mol?L£≠1 £®1∑÷£©
£Ω0.00067 mol?L£≠1 £®1∑÷£©
∑¥”¶ ±º‰£∫ £Ω
£Ω £Ω6.7min £®1∑÷£©
£Ω6.7min £®1∑÷£©
KMnO4µƒ∆Ωæ˘∑¥”¶ÀŸ¬ £∫
¶Õ(KMnO4)£Ω £Ω
£Ω £Ω1°¡10£≠4 mol?L£≠1?min£≠1 £®1∑÷£©
£Ω1°¡10£≠4 mol?L£≠1?min£≠1 £®1∑÷£©
£®“ª≤ΩÕÍ≥…º∆À„«“Ω·π˚’˝»∑µ√3∑÷£¨Ω·π˚¥ÌŒÛµ√0∑÷°£ÀŸ¬ µ•Œª¥ÌŒÛø€1∑÷£©
¢⁄ ∑Ò£®ªÚ£∫≤ªø…––£© £®1∑÷£© »°π˝¡øµƒÃª˝œýÕ¨°¢≈®∂»≤ªÕ¨µƒ≤ðÀ·»Ð“∫∑÷±Õ¨ ±”Îê˝œýÕ¨°¢≈®∂»œýÕ¨µƒ∏þ√ÃÀ·ºÿÀ·–‘»Ð“∫∑¥”¶°££®3∑÷£©
£®ª˘±æÀº¬∑¥ÌŒÛµ√0∑÷£¨Àº¬∑’˝»∑Œ¥«øµ˜≤ðÀ·π˝¡øø€1∑÷£¨Œ¥«øµ˜Ãª˝œýÕ¨ø€1∑÷£©
18


19£Æ£®12∑÷£©£®1£©‘ˆ¥Û £®1∑÷£©£®2£©≤ª“∆∂Ø £®1∑÷£©£®3£©£®4∑÷£©£®∏˜’º2∑÷£¨∆µ„Œª÷√°¢«˙œþ◊þ ∆°¢÷’µ„”Α≠«˙œþµƒœý∂‘∏þµÕµ»÷ª“™”–“ª¥¶¥ÌŒÛ‘Úµ√0∑÷°££©
£®4£©£®4∑÷£©0.60(2∑÷) ¶Õ’˝_>_¶ÕƒÊ£®2∑÷£©
£®5£©£≠787.0 £®2∑÷£©£®≤ª¥¯∏∫∫≈µ√0∑÷£¨”––ß ˝◊÷≤ª◊º»∑ø€1∑÷°££©
20£Æ£®√øø’2∑÷£¨π≤10∑÷£©
£®1£© (2∑÷) £®2£©æ˘Œ™—ıªØªπ‘≠∑¥”¶ (2∑÷)
(2∑÷) £®2£©æ˘Œ™—ıªØªπ‘≠∑¥”¶ (2∑÷)
£®3£©3Fe+ 4H2O  Fe 3O4+4H2°¸
(2∑÷)
Fe 3O4+4H2°¸
(2∑÷)
£®4£©Fe+6H£´+3NO3£≠£ΩFe3£´+3NO2°¸+3 H2O
3 Fe+8H£´+2NO3£≠£Ω3Fe2£´+2NO °¸+4H2O (π≤2∑÷)
£®5£©»°…Ÿ¡ø—˘∆∑”⁄ ‘πÐ÷–£¨º”»ÎKSCN»Ð“∫£¨»Áπ˚≥ˆœ÷∫Ï…´£¨Àµ√˜±‰÷ £ª∑¥÷Æ£¨√ª”–±‰÷ (2∑÷)
21£®1£©a°¢d(1∑÷)£ª £®2£©3:2:3(1∑÷)£ª £®3£©C3H4O4(1∑÷)£ª


 £®4£©
+ CH2(COOH) 2
+H2O(2∑÷)
£®4£©
+ CH2(COOH) 2
+H2O(2∑÷)
£®5£©4÷÷ (2∑÷) £®–¥≥ˆœ¬¡–Àƒ÷÷Ω·ππ÷–µƒ»Œ“‚“ª÷÷æ˘ø…µ√2∑÷£©
 |
22£Æ£®10∑÷£©£®1£© C F £®2∑÷£© £®¬©—°1∏ˆø€1∑÷£¨∂ý—°“ª∏ˆ“≤ø€1∑÷£¨ø€ÕÍŒ™÷π°££©
£®2£©¢Ÿ 3 £®1∑÷£© 2 £®1∑÷£©
¢⁄ HCO3£≠÷–∫¨”–O£≠Hº¸£¨œýª•÷ƺ‰ø…Õ®π˝O£≠H©©O«‚º¸µÞ∫œ£®1∑÷£©
£®–¥≥ˆHCO3£≠ªØ—ß Ω≤¢÷∏≥ˆ¿Î◊”÷ƺ‰”–«‚º¸◊˜”√≤≈ƒÐµ√∑÷£©
£®3£©∂œ¡—C°‘O÷–µƒ“ª∏ˆ¶–º¸œ˚∫ƒµƒƒÐ¡ø «273kJ/mol£¨∂œ¡—N°‘N÷–µƒ“ª∏ˆ¶–º¸œ˚∫ƒµƒƒÐ¡ø «523.3kJ/mol£¨ ∂œ¡—“ª∏ˆ¶–º¸CO±»N2∏¸»ð“◊£¨À˘“‘CO∏¸ªÓ∆√°££®2∑÷£©
 £®– ˆ«Â≥˛£¨Œ¥æþú∆À„≥ˆ ˝÷µ≤ªø€∑÷°££©
£®– ˆ«Â≥˛£¨Œ¥æþú∆À„≥ˆ ˝÷µ≤ªø€∑÷°££©
£®4£©¢Ÿ 1s22s22p63s23p63d84s2 £®1∑÷£©
¢⁄ ∑÷◊”æß࣮1∑÷£©
¢€ £®1∑÷£©
23£Æ(10∑÷) £®1£©FeC2O4?2H2O FeC2O4+2H2O£¨º”»» ºı…Ÿµƒ÷ ¡øµ»”⁄À˘∫¨Ω·æßÀƵƒ÷ ¡ø £®2£©FeO°¢CO°¢CO2£ª1£∫1£∫1°££®3£©30£•°££®4£©6Fe2O3
FeC2O4+2H2O£¨º”»» ºı…Ÿµƒ÷ ¡øµ»”⁄À˘∫¨Ω·æßÀƵƒ÷ ¡ø £®2£©FeO°¢CO°¢CO2£ª1£∫1£∫1°££®3£©30£•°££®4£©6Fe2O3 4Fe3O4+O2°¸
4Fe3O4+O2°¸
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com