
题目列表(包括答案和解析)
 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示. (2012?河西区一模)碳和碳的化合物在生产、生活中的应用非常广泛,此方面的科学研究为当今提倡的“低碳生活方式”提供依据.请按要求回答下列问题:
(2012?河西区一模)碳和碳的化合物在生产、生活中的应用非常广泛,此方面的科学研究为当今提倡的“低碳生活方式”提供依据.请按要求回答下列问题:
| ||
| ||
| 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | |
| N2 | 8.00 | 7.40 | 7.00 | 6.72 | 6.52 | 6.36 | 6.20 | 6.00 | 6.00 | 6.00 |
| CO | 0.00 | 1.80 | 3.00 | 3.84 | 4.22 | 4.92 | 5.40 |
 (1)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.①由图中所给数据进行分析,该反应的化学方程式为
(1)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.①由图中所给数据进行分析,该反应的化学方程式为 2Z
2Z 2Z
2Z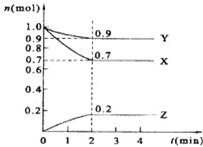 某温度时,在2L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示.
一、(本题包括18小题,共54分)
1.D2.C3.D4.C5.A6.D7.B8.B9. B 10. B 11. C 12. B 13.D14.A15.A16.A17.C18.B
二、(本题包括4小题,共16分)
1.(2分)(1)N2H4(l)+2H2O2(l)= N2 (g) +4H2O (g);△H=-640 kJ?mol-1
2.(4分)(1)TiCl4+2Mg=Ti+2MgCl2(2)―80 kJ?mol-1
3.(4分)(1) 3X+Y.files\image024.gif) 2Z (2) 0.05
2Z (2) 0.05
4.(6分)①大于或等于 ② > ③ A C
三、(本题包括2小题,共14分)
1. (5分)(1)0.05mol?L-1 (2)③ ⑸
2..(9分)(1)0.25(2)[H2] = 0.016mol?L-1,[HI]= 0.0080mol?L-1
四、(本题包括2小题,共16分)
1.(8分)(1)不能(2分);因为酚酞的变色范围为8~10,即pH范围呈碱性,而BaCO3需在酸性溶液中才会不断溶解。(2分)
(2)偏高(2分);因为甲基橙的变色范围的pH为3.1~4.4,当滴定到甲基橙由黄色变到橙色时,溶液的pH已经降到4.4以下,此时已有部分BaCO3与盐酸反应,故消耗的盐酸的量偏大。(2分)
2.(8分)(1)偏低 (2分)
(2)25%(3分)
(3)37.5%(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com