
题目列表(包括答案和解析)
(Ⅰ)(8分)某无色溶液中可能含有Na+、SO42— 、MnO4—、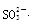 、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是 ;肯定没有的离子是 。
⑵写出步骤②中的离子方程式 。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
① ② 。
简述设计实验证明: 。
某无色溶液中可能含有Na+、SO42―、SO32―、Cl―、Br―、CO32―中的若干种,依次进行下列实验。观察到现象如下:①用pH试纸检验,溶液pH>7;②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置、CCl4层呈橙色,用分液漏斗分液;③向分液后的水溶液中加入Ba(NO3)2和HNO3的混合液,只有白色沉淀,过滤;④在滤液中加入AgNO3和HNO3的混合液,有白色沉淀产生。
回答下列问题:
(1)原溶液中肯定含有的离子是 ;肯定没有的离子是 。
(2)步骤③改用Ba(NO3)2和盐酸的混合液,对判断①有无影响?
。
(3)写出步骤②中的离子方程式 。
(Ⅰ)(8分)某无色溶液中可能含有Na+、SO42—
、MnO4—、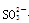 、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是 ;肯定没有的离子是 。
⑵写出步骤②中的离子方程式 。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
① ② 。
简述设计实验证明: 。
选择题(共72分)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
B
D
D
C
A
B
D
C
B
A
A
C
D
D
A
B
B
C
三、填空题(本大题共2小题,共18分)
.files\image010.gif) 19. (10分)
19. (10分)
(1) 2 FeCl3+ 1
H2S 2
FeCl2+ 1 S↓+ 2 HCl
(配平2分,电子方向1分,电子个数1分)
(2) 2Fe3++H2S=2Fe2++S↓+2H+ (2分)
(3) 22.4 (2分)
(4) Cl2>Fe3+>S(2分)
20.(8分)
(1) 8∶1 4∶1 2∶1
(2) 3∶4 (每空2分)
四、推断题(本大题共2小题,共29分)
21.(13分)
(1) Na+、I-、HCO3-; Cu2+ CO32-(每填对一种离子,给1分)
(2) Cl2+2I-=2Cl-+I2 HCO3-+H+ =CO2↑+ H2O(各2分)
(3) K+(2分)
透过蓝色钴玻璃观看,若火焰呈紫色则含有K+,否则不含K+(2分)
22.(16分) (各2分)
(1) A NaHCO3 , E Na2O2
(2) 2NaHCO3.files\image011.gif)
.files\image012.gif) Na2CO3 +CO2↑ + H2O
Na2CO3 +CO2↑ + H2O
2Na2O2 +2H2O = 4Na+ +4OH―+O2↑
(3) 2OH―+CO2 = CO32―+H2O
2Na + CO32―+ CO2 + H2O = 2NaHCO3↓
Ca2++ 2OH―+ 2HCO3―=CaCO3↓+ H2O + CO32-
(4) B
五、实验题(本大题共2小题,共21分)
23.(3分)①④⑥ (少选1个扣1分,错选一个扣一分)
24.(18分)(各2分)
(1) MnO2 + 4HCl(浓).files\image011.gif)
.files\image012.gif) MnCl2
+ Cl2↑+ 2H2O
MnCl2
+ Cl2↑+ 2H2O
(2) 饱和食盐水 浓硫酸 b
Cl2 + 2OH-= Cl-+ ClO-+ H2O
(3) 铜丝剧烈燃烧,生成棕黄色的烟 能 Mg>Al>Cu
(4) Cl-+ ClO-+ 2H+=Cl2↑+ H2O
六、计算题(本大题共1小题,共10分)
25.(10分)
(1) (6分)设碳酸钠和碳酸氢钠的物质的量分别为x和y
Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑+ H2O NaHCO3 + HNO3 = NaNO3 + CO2↑+ H2O
1 2 1 1 1 1
x 2 x x y y y
.files\image013.gif)
x
+ y =
解得:x = 0.05 mol y = 0.05 mol
∴ 碳酸钠和碳酸氢钠的物质的量分别为0.0500 mol和0.0500 mol
(方程式各1分,答案各2分)
(2) 消耗的硝酸的物质的量n(HNO3) = 2x + y = 0.15 mol
c(HNO3) = n(HNO3)÷V= 0.15
mol÷
(3) m(HNO3) = 0.15
mol×
m(溶液) =V?ρ= 25mL×
ω%= m(HNO3)÷m(溶液) =
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com