
题目列表(包括答案和解析)
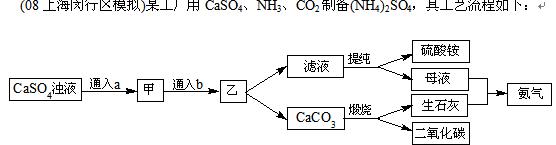
回答下列问题:
(1)硫酸铵在农业生产中的用途是____________,写出利用该流程制备的化学方程式:____________________________________________________________________。
(2)操作a和b应分别通入__________(填序号),选择该选项操作的理由是
。
A.足量CO2、适量NH3 B.足量NH3、适量CO2
C.适量CO2、足量NH3 D.适量NH3、足量CO2
(3)判断操作b通入的气体是适量还是过量的简单实验方法是_____________________
_____________________________________________________________________。
(4)上述流程中,可以循环使用的物质是_____________、____________(写化学式)。
(5)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是____________。
A.蒸干 B.蒸发 C.冷却结晶 D.过滤
(6)上述生成流程中,有关NH3的作用及说明正确的是______________。
A.提供制备所需的氮元素 B.增大CO32-的浓度促进反应发生
C.作反应的催化剂 D.生产1mol(NH4)2SO4,至少消耗2mol NH3
试回答下列问题:
(1)指出下面物质分子或离子的空间构型:PO43-____________________;CS2____________________。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式: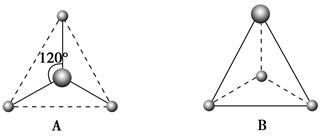
A:________________;B:________________。
(3)按要求写出第2周期非金属元素构成的中性分子的化学式:平面形分子________________,三角锥形分子________________,四面体形分子________________。
(4)下列一组微粒中键角由大到小顺序排列为________(用编号填写)
①HCN;②SiF4;③SCl2;④CO32-;⑤H3O+
试回答下列问题:
(1)指出下面物质分子或离子的空间构型:PO43-____________________;CS2____________________。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
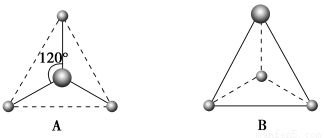
A:________________;B:________________。
(3)按要求写出第2周期非金属元素构成的中性分子的化学式:平面形分子________________,三角锥形分子________________,四面体形分子________________。
(4)下列一组微粒中键角由大到小顺序排列为________(用编号填写)
①HCN;②SiF4;③SCl2;④CO32-;⑤H3O+

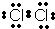
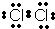
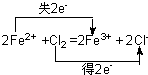
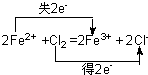
选择题(共72分)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
B
D
D
C
A
B
D
C
B
A
A
C
D
D
A
B
B
C
三、填空题(本大题共2小题,共18分)
.files\image010.gif) 19. (10分)
19. (10分)
(1) 2 FeCl3+ 1
H2S 2
FeCl2+ 1 S↓+ 2 HCl
(配平2分,电子方向1分,电子个数1分)
(2) 2Fe3++H2S=2Fe2++S↓+2H+ (2分)
(3) 22.4 (2分)
(4) Cl2>Fe3+>S(2分)
20.(8分)
(1) 8∶1 4∶1 2∶1
(2) 3∶4 (每空2分)
四、推断题(本大题共2小题,共29分)
21.(13分)
(1) Na+、I-、HCO3-; Cu2+ CO32-(每填对一种离子,给1分)
(2) Cl2+2I-=2Cl-+I2 HCO3-+H+ =CO2↑+ H2O(各2分)
(3) K+(2分)
透过蓝色钴玻璃观看,若火焰呈紫色则含有K+,否则不含K+(2分)
22.(16分) (各2分)
(1) A NaHCO3 , E Na2O2
(2) 2NaHCO3.files\image011.gif)
.files\image012.gif) Na2CO3 +CO2↑ + H2O
Na2CO3 +CO2↑ + H2O
2Na2O2 +2H2O = 4Na+ +4OH―+O2↑
(3) 2OH―+CO2 = CO32―+H2O
2Na + CO32―+ CO2 + H2O = 2NaHCO3↓
Ca2++ 2OH―+ 2HCO3―=CaCO3↓+ H2O + CO32-
(4) B
五、实验题(本大题共2小题,共21分)
23.(3分)①④⑥ (少选1个扣1分,错选一个扣一分)
24.(18分)(各2分)
(1) MnO2 + 4HCl(浓).files\image011.gif)
.files\image012.gif) MnCl2
+ Cl2↑+ 2H2O
MnCl2
+ Cl2↑+ 2H2O
(2) 饱和食盐水 浓硫酸 b
Cl2 + 2OH-= Cl-+ ClO-+ H2O
(3) 铜丝剧烈燃烧,生成棕黄色的烟 能 Mg>Al>Cu
(4) Cl-+ ClO-+ 2H+=Cl2↑+ H2O
六、计算题(本大题共1小题,共10分)
25.(10分)
(1) (6分)设碳酸钠和碳酸氢钠的物质的量分别为x和y
Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑+ H2O NaHCO3 + HNO3 = NaNO3 + CO2↑+ H2O
1 2 1 1 1 1
x 2 x x y y y
.files\image013.gif)
x
+ y =
解得:x = 0.05 mol y = 0.05 mol
∴ 碳酸钠和碳酸氢钠的物质的量分别为0.0500 mol和0.0500 mol
(方程式各1分,答案各2分)
(2) 消耗的硝酸的物质的量n(HNO3) = 2x + y = 0.15 mol
c(HNO3) = n(HNO3)÷V= 0.15
mol÷
(3) m(HNO3) = 0.15
mol×
m(溶液) =V?ρ= 25mL×
ω%= m(HNO3)÷m(溶液) =
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com