
题目列表(包括答案和解析)
(10分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A与D按原子个数比1﹕1或2﹕l形成常温下为液态的化合物,E也能与D按原子个数比1﹕1或2﹕l形成化合物,B的外围电子数为内层电子数的两倍,B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。请按要求回答以下问题:
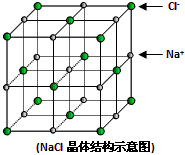
(1)上图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 , E与D按原子个数比1﹕1形成的化合物的电子式为 。
(2)人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F—D | F—F | B—B | F—B | C═D | D═D |
| 键能/kJ·mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
(10分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A与D按原子个数比1﹕1或2﹕l形成常温下为液态的化合物,E也能与D按原子个数比1﹕1或2﹕l形成化合物,B的外围电子数为内层电子数的两倍,B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。请按要求回答以下问题:
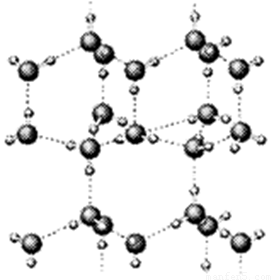
(1)上图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 , E与D按原子个数比1﹕1形成的化合物的电子式为 。
(2)人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
|
化学键 |
F—D |
F—F |
B—B |
F—B |
C═D |
D═D |
|
键能/kJ·mol-1 |
460 |
176 |
347.7 |
347 |
745 |
497.3 |
①下列三种物质形成的晶体,熔点由高到低的顺序(用a、b、c表示):
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②F单质晶体中一个F原子与其紧邻的F原子形成的空间构型为_____________,
③已知加热下可发生如下转化:
F(s) + D2(g) 加热 FD2(s)
根据上表数据计算F单质晶体发生上述反应的反应热△H为: 。
有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A与D按原子个数比1﹕1或
2﹕l形成常温下为液态的化合物,E也能与D按原子个数比1﹕1或2﹕l形成化合物,B的外围电子数为内层电子数的两倍,B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。请按要求回答以下问题:
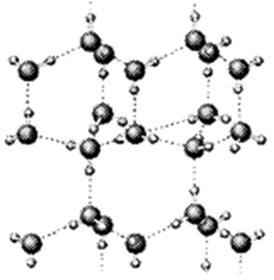
(1)右图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 , E与D按原子个数比1﹕1形成的化合物的电子式为 。
(2)人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F—D | F—F | B—B | F—B | C═D | D═D |
| 键能/kJ·mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
①下列三种物质形成的晶体,熔点由高到低的顺序(用a、b、c表示):
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②F单质晶体中一个F原子与其紧邻的F原子形成的空间构型为_____________,
③已知加热下可发生如下转化:
F(s) + D2(g) 加热 FD2(s)
根据上表数据计算F单质晶体发生上述反应的反应热△H为: 。
| 化学键 | F—D | F—F | B—B | F—B | C═D | D═D |
| 键能/kJ·mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
选择题(共72分)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
B
D
D
C
A
B
D
C
B
A
A
C
D
D
A
B
B
C
三、填空题(本大题共2小题,共18分)
.files\image010.gif) 19. (10分)
19. (10分)
(1) 2 FeCl3+ 1
H2S 2
FeCl2+ 1 S↓+ 2 HCl
(配平2分,电子方向1分,电子个数1分)
(2) 2Fe3++H2S=2Fe2++S↓+2H+ (2分)
(3) 22.4 (2分)
(4) Cl2>Fe3+>S(2分)
20.(8分)
(1) 8∶1 4∶1 2∶1
(2) 3∶4 (每空2分)
四、推断题(本大题共2小题,共29分)
21.(13分)
(1) Na+、I-、HCO3-; Cu2+ CO32-(每填对一种离子,给1分)
(2) Cl2+2I-=2Cl-+I2 HCO3-+H+ =CO2↑+ H2O(各2分)
(3) K+(2分)
透过蓝色钴玻璃观看,若火焰呈紫色则含有K+,否则不含K+(2分)
22.(16分) (各2分)
(1) A NaHCO3 , E Na2O2
(2) 2NaHCO3.files\image011.gif)
.files\image012.gif) Na2CO3 +CO2↑ + H2O
Na2CO3 +CO2↑ + H2O
2Na2O2 +2H2O = 4Na+ +4OH―+O2↑
(3) 2OH―+CO2 = CO32―+H2O
2Na + CO32―+ CO2 + H2O = 2NaHCO3↓
Ca2++ 2OH―+ 2HCO3―=CaCO3↓+ H2O + CO32-
(4) B
五、实验题(本大题共2小题,共21分)
23.(3分)①④⑥ (少选1个扣1分,错选一个扣一分)
24.(18分)(各2分)
(1) MnO2 + 4HCl(浓).files\image011.gif)
.files\image012.gif) MnCl2
+ Cl2↑+ 2H2O
MnCl2
+ Cl2↑+ 2H2O
(2) 饱和食盐水 浓硫酸 b
Cl2 + 2OH-= Cl-+ ClO-+ H2O
(3) 铜丝剧烈燃烧,生成棕黄色的烟 能 Mg>Al>Cu
(4) Cl-+ ClO-+ 2H+=Cl2↑+ H2O
六、计算题(本大题共1小题,共10分)
25.(10分)
(1) (6分)设碳酸钠和碳酸氢钠的物质的量分别为x和y
Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑+ H2O NaHCO3 + HNO3 = NaNO3 + CO2↑+ H2O
1 2 1 1 1 1
x 2 x x y y y
.files\image013.gif)
x
+ y =
解得:x = 0.05 mol y = 0.05 mol
∴ 碳酸钠和碳酸氢钠的物质的量分别为0.0500 mol和0.0500 mol
(方程式各1分,答案各2分)
(2) 消耗的硝酸的物质的量n(HNO3) = 2x + y = 0.15 mol
c(HNO3) = n(HNO3)÷V= 0.15
mol÷
(3) m(HNO3) = 0.15
mol×
m(溶液) =V?ρ= 25mL×
ω%= m(HNO3)÷m(溶液) =
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com