
题目列表(包括答案和解析)
2.7g铝粉分别与体积均为100mL、浓度均为2mol/L的(1)硫酸溶液、(2)烧碱溶液、(3)盐酸完全反应,放出氢气的体积关系(相同条件)是
A.(1)=(2)=(3) B.(1)=(2)>(3)
C.(1)>(2)>(3) D.(2)>(1)=(3)
利用所学化学反应原理,解决以下问题:
(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、![]() 、Cl一四种离子,且c(
、Cl一四种离子,且c(![]() )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是_____________。
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是_____________。
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:______________________。
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是_____________。
(4)以石墨电极电解100 mL 0.1mol·L-1CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为__________g。
(5)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如右图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=_______mol·L-1.
(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+I2(g)![]() 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:
下列说法正确的是_______________。
A.![]() +
+![]() =1 B.2
=1 B.2![]() =
=![]() C.a+b=14.9 D.c1=c2=c3
C.a+b=14.9 D.c1=c2=c3
在下列各说法中,正确的是 ( )
A.△H > 0表示放热反应,△H < 0表示吸热反应
B.热化学方程式中的化学计量数表示物质的量,可以是分数
C.1 mol H2SO4与1 molBa(OH)2反应生成BaSO4沉淀时放出的热量叫做中和热
D.1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热
(10分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K= 。(保留2位小数)
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。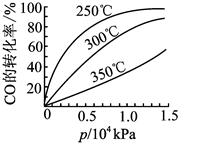
该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
选择题(1―10题每小题2分,11-25题每小题3分,共65分)
题目
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
B
D
C
B
D
A
B
D
A
A
D
A
C
题目
14
15
16
17
18
19
20
21
22
23
24
25
答案
C
B
C
D
B
A
C
C
B
D
C
C
三、填空题(共35分,除注明分数外,其余每个给分点为1分)
26.(6分)(1)10+m 8 (2)28+n 36 (3)离子键 (4)

27.(9分)(1)Mg O (2)Na>Mg>C>O>H (3)Mg(OH)2<NaOH
(4)H2O2、Na2O2、O3、C(活性炭)等任意三个
(5)(2分)NaHCO3+H2O NaOH+H2CO3
NaOH+H2CO3
28.(7分)(1)Cu2+、Ba2+、Fe3+ (2)AlO2-、HCO3-、SO42-、Na+
29.(13分)(1)H2O2 MnO2
(2)2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O 溶液由无色变橙色
(3)①CaO+H2O==Ca(OH)2,反应放热,NH3?H2O NH3↑+H2O
NH3↑+H2O
②用玻璃棒蘸取少许浓盐酸靠近收集NH3的烧瓶口,若产生白烟,说明烧瓶已收集满NH3,反之,则没有收集满或用湿润的红色石蕊试纸变蓝,则说明NH3已收集满,反之,则没有收集满
(4)①挤出胶头滴管中的水(1分),打开止水夹(1分),
极易溶解于水(1分)和其水溶液呈碱性(1分)
② (2分)
(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com