
题目列表(包括答案和解析)
(1)写出硫酸铝铵在水溶液中的电离方程式: 。?
若将硫酸铝铵溶液加入水稀释,物质的量浓度上升的离子是 (填离子符号)。?
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀?
②有刺激性气味的气体放出?
③白色沉淀量逐渐增多?
④白色沉淀完全消失
⑤白色沉淀逐渐减少
请排出以上各种现象由先到后出现的正确顺序 (用序号回答)。?
(3)请写出有关反应的离子方程式:
① 。?
② 。?
③ 。
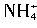 与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应:
与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应: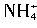 +[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答:
+[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答: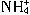 与Al
与Al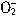 在水溶液中不能大量共存,会发生如下反应:
在水溶液中不能大量共存,会发生如下反应: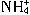 +Al
+Al +H2O=Al(OH)3↓+NH3↑。试回答:
+H2O=Al(OH)3↓+NH3↑。试回答:在化工生产中,要用到一种无色、易溶于水的晶体 铝铵矾,该晶体是一种复盐,其主要化学成分为十二水硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化,已知NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:
铝铵矾,该晶体是一种复盐,其主要化学成分为十二水硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化,已知NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:
NH4++AlO2-+H2O=Al(OH)3↓+NH3↑;试回答:
(1)写出硫酸铝铵在水溶液中电离的方程式:________;若将硫酸铝铵溶液加入水稀释,物质的量浓度上升的离子是________(填离子符号)
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;
④白色沉淀完全消失;⑤白色沉淀逐渐减少.请排出以上各种现象由先到后出现的正确顺序(用序号回答)________;
(3)请写出有关反应的离子方程式:
①________
②________
③________
1
2
3
4
5
6
7
8
C
A
B
C
D
D
B
C
9
10
11
12
13
14
15
16
C
D
B
B
D
D
C
B
17.(9分) (1)C4H4; 1。(每空1分,共2分)
(2)D。(1分) (3) 。(2分) (4)
。(2分) (4)  ,
, (每空2分,共4分,合理即给分)。
(每空2分,共4分,合理即给分)。
18、(8分)答案:(1)< 变小 (2)增大 不变 变小(3)A (每空1分,共6分)
(4)0.02mol(2分)
19.(8分)(1)①→③→②→⑤→④;
(2)①Al3++3OH-=Al(OH)3↓②NH4++OH-=NH3↑+H2O
③Al(OH)3+OH-=AlO2-+2H2O
20.(9分)(1)CO2(1分) 直线型 (1分)
(2)CaC2+N2=CaCN2+C(2分) 30(1分)
(3)将粗产品溶于热水中并趁热过滤,冷却待溶液中有大量晶体析出时再过滤(2分)
(若是先将粗产品溶于冷水并过滤,将所得固体再溶于热水,冷却结晶再过滤,只给1分)
(4)三聚氰胺为白色结晶粉末,没有什么气味和味道(2分)
21.(10分)(1)加热 ,Fe表面被浓硝酸钝化(每空1分,共2分)
(2)F→G+X :3NO2+H2O=2HNO3+NO , G→F : 2NO+O2=2NO2
(3)白色固体迅速变为灰绿色,最后变为红褐色,
有关的化学方程式是 4Fe(OH)2+2H2O+O2=4Fe(OH)3 (每空2分,共8分)
22. (8分)(1) C6H10 (3分) CH2=CH-CH2-CH2-CH=CH2 (2分)
 |
(2) (3分)
高二年级化学期末试卷参考答案
1
2
3
4
5
6
7
8
C
A
B
C
D
D
B
C
9
10
11
12
13
14
15
16
C
D
B
B
D
D
C
B
17.(9分) (1)C4H4; 1。(每空1分,共2分)
(2)D。(1分) (3) 。(2分) (4)
。(2分) (4)  ,
, (每空2分,共4分,合理即给分)。
(每空2分,共4分,合理即给分)。
18、(8分)答案:(1)< 变小 (2)增大 不变 变小(3)A (每空1分,共6分)
(4)0.02mol(2分)
19.(8分)(1)①→③→②→⑤→④;
(2)①Al3++3OH-=Al(OH)3↓②NH4++OH-=NH3↑+H2O
③Al(OH)3+OH-=AlO2-+2H2O
20.(9分)(1)CO2(1分) 直线型 (1分)
(2)CaC2+N2=CaCN2+C(2分) 30(1分)
(3)将粗产品溶于热水中并趁热过滤,冷却待溶液中有大量晶体析出时再过滤(2分)
(若是先将粗产品溶于冷水并过滤,将所得固体再溶于热水,冷却结晶再过滤,只给1分)
(4)三聚氰胺为白色结晶粉末,没有什么气味和味道(2分)
21.(10分)(1)加热 ,Fe表面被浓硝酸钝化(每空1分,共2分)
(2)F→G+X :3NO2+H2O=2HNO3+NO , G→F : 2NO+O2=2NO2
(3)白色固体迅速变为灰绿色,最后变为红褐色,
有关的化学方程式是 4Fe(OH)2+2H2O+O2=4Fe(OH)3 (每空2分,共8分)
22. (8分)(1) C6H10 (3分) CH2=CH-CH2-CH2-CH=CH2 (2分)
 |
(2) (3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com