
题目列表(包括答案和解析)

②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_________________。定容,摇匀。将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度
(6)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会__________(填“偏高”、“偏低”或“无影响”)。
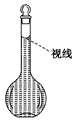
(7分)实验室欲用固体NaCl配制500 mL2 .0mol/L的NaCl溶液,试回答:
(1)实验室现在提供了如下仪器,其中不用的仪器是(用字母表示)___ _____,还缺少的玻璃仪器是(填仪器名称) 。
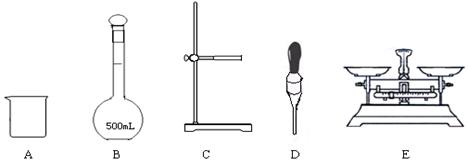 |
(2)配制时应称取NaCl________ g。
(3)配制过程有如下操作,溶解并转移溶液后的下一步操作是(用字母表示,下同) ,定容后的下一步操作是 。
A.冷却 B.称量 C.计算 D.定容 E.溶解
F.倒转摇匀 G.转移溶液 H.洗涤烧杯并将洗涤液转移到容量瓶
(4)①若先用蒸馏水润洗容量瓶,再转移溶液,则实验结果将(填“偏大”、“偏小”或“不受影响”,下同)______ ;
②若定容时俯视刻度线,则实验结果将_______ _。
(16分)
Ⅰ.下列操作正确的是_______.
A、用氨水清洗做过银镜反应的试管
B、用酒精清洗有硫沉淀的试管
C、用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
E、如果苯酚浓溶液沾到皮肤上,应立即用70℃以上的水清洗
F、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
G、用托盘天平称取10.50 g干燥的NaCl固体;
H、向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
I、配制Al2(SO4)3溶液时,加入少量的稀硫酸。
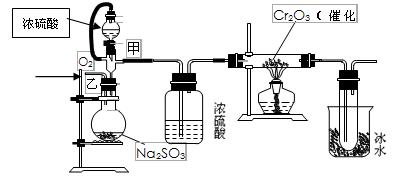
Ⅱ.用下图装置进行SO2转化为SO3的转化率测定实验:
(1)写出圆底烧瓶中发生反应的化学方程式
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程) 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。
(4)本实验装置设计中有不恰当的地方,请指出: 。
所增加装置的目的是 。
(5)将反应生成的44.8L(标况下)SO2气体全部通过硬质玻璃管后,在右侧烧杯的试管中得到152g固体,则SO2的转化率为
(16分)
Ⅰ.下列操作正确的是_______.
| A.用氨水清洗做过银镜反应的试管 |
| B.用酒精清洗有硫沉淀的试管 |
| C.用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液; |
| D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
(16分)
Ⅰ.下列操作正确的是_______.
A、用氨水清洗做过银镜反应的试管
B、用酒精清洗有硫沉淀的试管
C、用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
E、如果苯酚浓溶液沾到皮肤上,应立即用70℃以上的水清洗
F、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
G、用托盘天平称取10.50 g干燥的NaCl固体;
H、向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
I、配制Al2(SO4)3溶液时,加入少量的稀硫酸。
Ⅱ.用下图装置进行SO2转化为SO3的转化率测定实验:
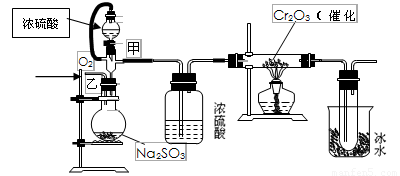
(1)写出圆底烧瓶中发生反应的化学方程式
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程) 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。
(4)本实验装置设计中有不恰当的地方,请指出: 。
所增加装置的目的是 。
(5)将反应生成的44.8L(标况下)SO2气体全部通过硬质玻璃管后,在右侧烧杯的试管中得到152g固体,则SO2的转化率为
一、选择题(每小题3分,w.w.w.k.s.5 u.c.o.m共45分)
题号
 1
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
D
D
C
B
B
D
B
B
C
D
A
A
D
B
C
二、填空题(本题共30分,化学方程式、离子方程式每个2分,其余每空1分)
16.(共3分)② ④ ① …………………………………………………(每空1分,共3分)
17.(共4分)是否单质 Mg、O2 、N2 是否气体 Mg (其它合理答案也可)
……………………………………………………………………(每空1分,共4分)
18.(共6分)小苏打 碳酸氢钠 CO2 + 2OH- = H2O + CO32-;
H+ + HCO3- = H2O+ CO2↑;…………………………(方程式2分,其它每空1分)
19.(共6分)
②(1分);Cu+4HNO3= Cu(NO3)2+ 2NO2↑+ 2H2O………………………………(2分)
⑤(1分);Al2O3+2NaOH=2NaAlO2+2H2O………………………………………(2分)
20.(共5分)(1)①FeCl2、③HCl、⑤Cl2 ………………………(每空1分,共3分)
(2)2Fe2++Cl2=2Fe3++2Cl-……………………………………………………………(2分)
21.(共6分)(1)红棕色………………………………………………………………(1分)
(2)NO(1分 ) ;2NO+O2=2NO2………………………………………………(2分)
(3)NO2中氮的化合价为+4,生成的NO中氮的化合价为+2,氮元素被还原,在其他元素不变价的情况下,酸中的氮元素应被氧化升价。…………………………(1分)
(4)一氧化氮与水中的氧气反应,生成二氧化氮被水吸收生成硝酸。…………(1分)
三、实验题(本题共15分)
22.(本题共7分)(1)C 玻璃棒…………………………………………(每空1分,共2分)
(2)58.5……………………………………………………………………………………(1分)
(3) H ; F…………………………………………………………………(每空1分,共2分)
(4)①不受影响 ②偏大…………………………………………………(每空1分,共2分)
23.(本题共8分)
(1)②(1分);无污染空气的SO2生成,节约H2SO4……………………………………(2分)
(2)品红褪色 SO2具有漂白性 不相同……………………………(每空1分,共3分)
(3)加热无色溶液看是否恢复红色,若恢复则气体为二氧化硫,若不恢复,气体为氯气(2分)
四、计算题(本题共10分)
24.(本题共4分)
(1)180g/mol ………………………………………………………………………………(2分)
(2)0.56mol/L………………………………………………………………………………(2分)
25.(本题共6分)
解:设能生成氢气在标况下的体积为x,生成氢氧化钠的物质的量为y。
2Na + 2H2O = 2NaOH + H2↑ ……………………………(1分)
 …………(1分)
…………(1分)
 …………………(1分)
…………………(1分)
x =
溶液中钠离子的物质的量浓度=(0.10mol+ 1.00mol/L 
答: 生成氢气在标况下的体积为1.12L,溶液中钠离子的物质的量浓度为1.50mol/L。
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com