
题目列表(包括答案和解析)
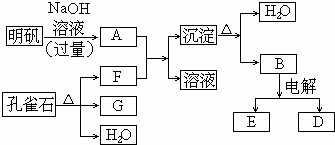 在一定条件下可实现下图所示物质之间的变化:
在一定条件下可实现下图所示物质之间的变化:
| ||
| ||
| ||
| ||

请填写下列空白:(提示:2Al2O3![]() 4Al+3O2↑)
4Al+3O2↑)
(1)孔雀石的主要成分是Cu2(OH)2CO3(碱式碳酸铜),受热易分解,上图中的F是____________。
(2)写出明矾与过量NaOH溶液反应的离子方程式:________________________________。
(3)图中所得G和D都是固体,混合后在高温下可发生反应,写出该反应的化学方程式:_________________________________________________________________。
(4)每生成1 mol D,同时生成_______________mol E。
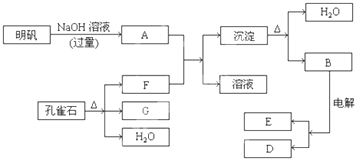
请填写以下空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,上图中的F是____________。
(2)写出明矾溶液与过量的NaOH溶液反应的离子方程式___________________。
(3)图中所得G和D都是固体,混合后在高温下可发生反应,写出该反应的化学方程式:_____________________________。
(4)每生成1 mol D,同时生成____________mol E。

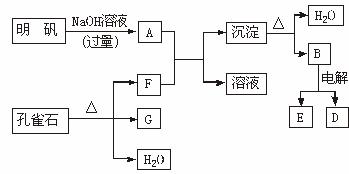
请填写下列空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,图中的F是___________(写化学式)。
(2)写出明矾与过量NaOH溶液反应的离子方程式:________________________。
(3)图中所得G和D都为固体,混合后在高温下可发生反应,写出该反应的化学方程式:
_____________________________________________ 。
(每题2分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
C
A
A
B
B
B
B
A
题号
11
12
13
14
15
16
17
18
19
20
答案
B
C
A
D
B
D
C
B
C
C
21.(每空1分,共3分)ClO- 和 Cl-; 1
22.(6分,每空2分)(1)Na2SiO3+ CO2+ H2O= H2SiO3↓+ Na2CO3
(2)Na2SiO3+2HCl= H2SiO3↓+ 2NaCl
(3)Na2CO3+2HCl= 2NaCl+ CO2↑+ H2O
23.(4分,每空1分)A:CaBr2;B:AgNO3;C:CuSO4;D:K2CO3。
24.(7分,其中⑴2分,其余每空1分)⑴ ;
沸腾炉
;
沸腾炉
(2)SO3、SO2、O2;C、B、A (3)98%浓硫酸,接触室
25.(8分,每空2分) (1)CO2
(2)Al3++4OH- = AlO2-+ 2H2O
(3)2Al+3CuO 3Cu+Al2O3
3Cu+Al2O3
(4)0.75
26.(每空1分,共7分)
(1)甲 丙 戊
(2)乙 有较多气泡放出的为稀硫酸
(3)丁 浓硫酸不具有挥发性
27.(10分,其中(3)4分,(4)2分,其余每空1分)
(1)乙 亚铁盐在空气中易被氧气氧化 (2) 还原
(3) 2Fe2++H2O2+2H+=2Fe3++2H2O Fe3++3SCN-=Fe(SCN)3 。
(4)再加过量KSCN,如果变血红色,则第二种合理;如果不变色,则第一种合理 (5) 未能测其成分。
28.(7分,其中(1)3分,(2)4分) (1)3分 (2)55.79%
29.(8分)
(2分)(1)Al3+ + 3OH―= Al (OH)3↓;Al (OH)3 + OH―= AlO2―+ 2H2O
(6分)(2)1.5 mol?L―1或3.5 mol?L―1
已知:n (AlCl3)
=  = 0.1mol (1分)
= 0.1mol (1分)
n (Al (OH)3) =  = 0.05mol (1分)
= 0.05mol (1分)
①NaOH溶液不足 Al3+ + 3OH―= Al (OH)3↓
0.15mol 0.05mol
c (NaOH) =  = 1.5 mol?L―1 (2分)
= 1.5 mol?L―1 (2分)
②NaOH溶液过量Al3+ + 3OH―= Al (OH)3↓ Al (OH)3 + OH―= AlO2―+ 2H2O
0.1mol 0.3mol 0.1mol 0.05mol 0.05mol
c (NaOH) =  = 3.5 mol?L―1(2分)
= 3.5 mol?L―1(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com