
题目列表(包括答案和解析)
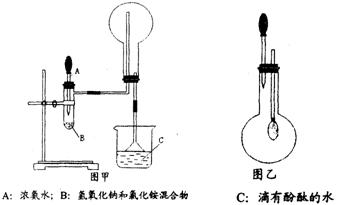
(I) 下图甲和乙是某学校王老师制备NH3 并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL 浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.

将上述中收满NH3 的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O ,此时小气球系在玻璃棒上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3 的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该化学方程式为:__________________________________________________________
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是__________。
①在NH3 · H2O 中有平衡![]() 使平衡向左移动
使平衡向左移动
②在NH3· H2O 中有平衡![]() 使平衡向左移动
使平衡向左移动
③Na0H 溶于水时放热,使体系的温度升高,NH3 的溶解度减小
④NH4Cl与NaOH 在此情况下可反应生成NH3,![]()
⑤NH4Cl 会分解释放出NH3
(3)图甲中的NH4Cl 与NaOH 固体混合物能否用CaO 固体代替 (填”能”与”不能”)
(4)如何判断图甲中烧瓶己收满NH3 ?_____________________________________________
(5)图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是 它说明了NH3

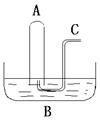
(Ⅱ)如上图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL,则原混合气体中NO2和NO的物质的量之比为
通过导气管C往余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是:
___________________________________________________
有关反应的化学方程式为:___________________________________________
当试管A中充满气体时停止通入氧气,然后将试管取出水槽,则共通入氧气的体积为 ________mL,水槽B中溶液的物质的量浓度为 mol·L-1(设溶液的体积仍为500 mL)
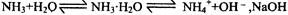 使平衡向左移动
使平衡向左移动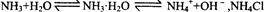 使平衡向左移动
使平衡向左移动
将上述收满NH3的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2 mL H2O,此时小气球系在玻璃管上呈自然松弛状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质。按要求回答下列问题:

(1)中学化学教材中是通过固体物质间加热反应来制取NH3的,该化学方程式为:
________________________________________________________________。
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是_________________。
①在NH3·H2O中有平衡NH3+H2O![]() NH3·H2O
NH3·H2O![]()
![]() +OH-,NaOH使平衡向左移动
+OH-,NaOH使平衡向左移动
②在NH3·H2O中有平衡NH3+H2O![]() NH3·H2O
NH3·H2O![]()
![]() +OH-,NH4Cl使平衡向左移动
+OH-,NH4Cl使平衡向左移动
③NaOH溶于水时放热,使体系的温度升高,NH3的溶解度减小
④NH4Cl与NaOH在此情况下可反应生成NH3,即![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
⑤NH4Cl会分解释放出NH3
(3)图甲中的NH4Cl与NaOH固体混合物能否用CaO固体代替__________(填“能”与“不能”)
(4)如何判断图甲中烧瓶已收满NH3? _______________________________________________。
(5)图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是_______________________________,它说明了NH3________________________________________________________。
Ⅱ.如图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.

通过导气管C往余下0.5a mL气体的试管A中通入氧气,当试管A中充满液体时停止通入氧气,则共通入氧气的体积为__________mL,然后将试管取出水槽,水槽B中溶液的物质的量浓度为_________mol·L-1(设溶液的体积仍为500 mL)。
(生物部分)
1-5 DDBCC
30.(20分,每空2分)
(1)①45 ②B ③26 87
(2)①有囊膜和刺突 糖蛋白
②(正)反馈
③以病毒核酸为模板,利用宿主细胞内原料合成的抗原分子
④溶酶体酶 通透性.渗透压
31. (22分)
(1)光照强度(2分)
CO2(或NaHCO3溶液)、温度、PH值、黑藻(2分,要求至少答出两项)
(2)读量筒中收集到的水的体积(2分)
(3)(3分,坐标轴标识2分、绘图2分)

(4)黑藻自身的呼吸作用会消耗氧气(4分)
(5)在20―200W范围内随着光照强度的不断升高,光合作用产生的氧气量也在升高,但光照强度达500W时氧气量反而降低,说明适度提高光照强度可以提高光合作用的强度。(4分,分析2分,结论2分)
(6)在100-500W范围内设置多组梯度进行实验。(4分,范围及梯度各2分)
荆州中学高三上学期期末理综卷
参考答案
(化学部分)
6-13CDCBD BDD
26.(14分)⑴A. NaHSO4 B. MgSO
⑵2H++SO42-+Ba2++2OH-====BaSO4↓+2H2O
⑶NH4NO3(s)====2H2O(g)+N2(g)+1/202(g);ΔN=-119.2kJ/mol
 27.(16分)⑴VIA ⑵S
27.(16分)⑴VIA ⑵S
⑶
⑷< NH4++H2O NH3?H2O+H+
NH3?H2O+H+
⑸金属质量 N元素或原子,电子得失(或化合价升降),金属与硝酸的反应
28.(15分)⑴Mg(2分) 直线形(2分)
⑵催化剂,加热(2分)
⑶将D溶液在HCl气流中蒸干(3分)
⑷2NH42+2e-===2NH3↑+H2↑(3分)
⑸2Mg+CO2 2MgO+C(3分)
2MgO+C(3分)
荆州中学高三上学期期末理综卷
参考答案
(物理部分)
14 A 15 C 16 AC 17. B 18.D 19 BD 20 C 21 D
22 Ⅰ、电流表外接,滑动变阻器限流、分压都可 Ⅱ、 229Ω(220~237Ω均算正确)
Ⅲ 、 0.800cm 0.194cm Ⅳ、 8.46×10-2Ωm (8.16×10-2 ~ 8.76×10-2Ωm均可)
23.由牛顿第二定律有 a =  m/s2 向左 , 球从10m/s 减速到0
m/s2 向左 , 球从10m/s 减速到0
运动S1 =  需的时间 t1 =
需的时间 t1 =  s
s
在F作用的最后 1 s,因 F >
Fu ,球向左加速 a2 =
 m/s2 向左
m/s2 向左
在这1s 内,球的位移 S =  = 0.5m 达到 v3 = a2t = 1 m/s 向左
= 0.5m 达到 v3 = a2t = 1 m/s 向左
撤去力 F 后球减速到停止 a3 =  m/s2
m/s2
得球又向左运动S =  m 故总位移为 S = S1?S2?S3 = 9.25
m
m 故总位移为 S = S1?S2?S3 = 9.25
m
24 铜块压缩弹簧到最短的过程中,系统动量守恒、mv0 = ( m +M )v
能量守恒  Wf =
Wf =  + Epm
+ Epm
铜块回到右端过程中系统有满足动量守恒( m +M )v = (m + M )v/
能量守恒
 + Epm - Wf =
+ Epm - Wf = 
得 Wf = Epm
故
EPm= 
25 设圆半径为R ,粒子电量为q 质量为 m
粒子匀速穿过场区时 qE = q v0B
2 R = v0 T0
撤去磁场,粒子在电场中做类平抛运动
由几何关系得 x = 3 R/2 = v0t1
故 t1/T0 = 3 /4
撤去电场后粒子在磁场中做匀速圆周运动,设半径为 r,周期为 T
由qv0B = mv02/r 得
r = mv0 /qB T = 2πm/qB
由几何关系有 r =
 tan
tan =
= 
所以 t2 = 
故 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com