实验题
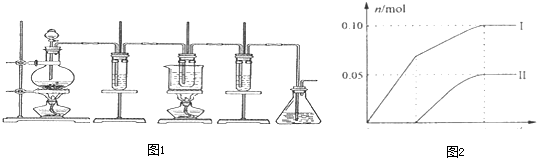
如图所示,是制取氯气并探究氯气的性质的实验装置.图1中:①氯气发生装置;②溴化亚铁溶液;③15mL 30% KOH溶液,并置于水浴中;④石灰乳;⑤尾气吸收装置.已知:氯气和碱的反应为放热反应.温度较高时,氯气和碱还能发生如下反应:
3Cl
2+6OH
-5Cl
-+ClO
3-+3H
2O
(1)实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有
B
B
(填写下列编号字母)的净化装置.
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)通入足量氯气后,②中反应的化学方程式为
3Cl2+2FeBr2=2FeCl3+Br2
3Cl2+2FeBr2=2FeCl3+Br2
,实验结束后,将②中液体与适量CCl
4溶液混合,充分静止、振荡,现象为
分层,上层水层黄色,下层有机层橙红色
分层,上层水层黄色,下层有机层橙红色
.
(3)利用③反应后的溶液可制备KClO
3晶体,实验过程:溶液→蒸发浓缩→冷却结晶→过滤→洗涤→干燥→氯酸钾晶体.蒸发浓缩时,当
出现少量晶体
出现少量晶体
时,应停止加热;洗涤时,如何检验晶体已洗涤干净(请简述操作方法):
取最后一次洗涤液,加入硝酸酸化的硝酸银,不产生白色沉淀则干净
取最后一次洗涤液,加入硝酸酸化的硝酸银,不产生白色沉淀则干净
.
(4)④的产物中Ca(ClO)
2的质量明显小于理论值.为探究产物的组成,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,ClO
-、ClO
3-两种离子的物质的量(n)与反应时间(t)的关系曲线如图2所示(不考虑氯气和水的反应).则图2中曲线I表示
ClO-
ClO-
离子的物质的量随反应时间变化的关系,所取石灰乳中含有Ca(OH)
2的物质的量为
0.25
0.25
mol.


 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2