(2012?西城区一模)工业上以粗食盐(含有少量Ca
2+、Mg
2+杂质)、氨、石灰石等为原料,可以制备Na
2CO
3.其过程如图1所示.
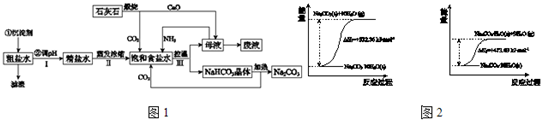
请回答:
(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有
CaCO3、Mg(OH)2
CaCO3、Mg(OH)2
.
(2)将CaO投入含有大量的NH
4Cl的母液中,能生成可循环使用的NH
3,该反应的化学方程式是
2NH4Cl+CaO=CaCl2+2NH3↑+H2O
2NH4Cl+CaO=CaCl2+2NH3↑+H2O
.
(3)向饱和食盐水中首先通入的气体是
NH3
NH3
,过程Ⅲ中生成NaHCO
3晶体的反应的化学方程式是
NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl
NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl
.
(4)碳酸钠晶体失水的能量变化示意图如图2:
Na
2CO
3?H
2O (s) 脱水反应的热化学方程式是
Na2CO3?H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1
Na2CO3?H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73kJ?mol-1
.
(5)产品纯碱中常含有NaCl.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体.则该产品中Na
2CO
3的质量分数是
.
(6)熔融Na
2CO
3可作甲烷--空气燃料电池的电解质,该电池负极的反应式是
CH4-8e-+4CO32-=5CO2+2H2O
CH4-8e-+4CO32-=5CO2+2H2O
.

