
题目列表(包括答案和解析)
以海水中常见物质NaCl为原料可以发展很多种工业,
(1)写出电解饱和食盐水的化学方程式______________________。
(2)以氯碱工业中的某些物质为原料制取漂白粉的化学方程式是_______________________
(3)从海水中获取的食盐中通常含有少量的MgCl2、Na2SO4等杂质,现采取下列方案将其提纯,其合理的操作顺序是__________________________________
①取一定量的食盐晶体溶于水 ②加入过量的NaOH溶液 ③加入过量的BaCl2溶液
④过滤 ⑤蒸发溶液 ⑥加入过量的Na2CO3溶液 ⑦加入适量的盐酸,调节溶液的pH
Ⅱ:2007年11月18日凌晨乌克兰一煤矿因瓦斯爆炸而发生矿难,死亡人数超过100人;2007年12月12日,河南省某煤矿因发生煤矿瓦斯突发事故而导致12名矿工遇难.瓦斯是CH4和CO混合而成的有毒气体,遇到明火极易发生爆炸
(4)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比
(5)已知在101kPa时,CO的燃烧热为283kJ/mol,相同条件下若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,写出CH4完全燃烧的热化学方程式
120℃,101kPa下,aml由CO、CH4组成的混合气体在bmlO2中完全燃烧后,恢复到原温度和压强
(6)若混合气体和O2恰好完全反应,产生bmlCO2,则混合气体中CH4的体积分数为
(7)若燃烧后气体体积缩小了a/4ml,写出a与b必须满足的关系式
以海水中常见物质NaCl为原料可以发展很多种工业,
(1)写出电解饱和食盐水的化学方程式______________________。
(2)以氯碱工业中的某些物质为原料制取漂白粉的化学方程式是_______________________
(3)从海水中获取的食盐中通常含有少量的MgCl2、Na2SO4等杂质,现采取下列方案将其提纯,其合理的操作顺序是________________________________
①取一定量的食盐晶体溶于水 ②加入过量的NaOH溶液 ③加入过量的BaCl2溶液
④过滤 ⑤蒸发溶液 ⑥加入过量的Na2CO3溶液 ⑦加入适量的盐酸,调节溶液的pH
Ⅱ:2007年11月18日凌晨乌克兰一煤矿因瓦斯爆炸而发生矿难,死亡人数超过100人;2007年12月12日,河南省某煤矿因发生煤矿瓦斯突发事故而导致12名矿工遇难.瓦斯是CH4和CO混合而成的有毒气体,遇到明火极易发生爆炸
(4)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比
(5)已知在101kPa时,CO的燃烧热为283kJ/mol,相同条件下若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,写出CH4完全燃烧的热化学方程式
120℃,101kPa下,a ml由CO、CH4组成的混合气体在bmlO2中完全燃烧后,恢复到原温度和压强
(6)若混合气体和O2恰好完全反应,产生bmlCO2,则混合气体中CH4的体积分数为
(7)若燃烧后气体体积缩小了a/4ml,写出a与b必须满足的关系式
以海水中常见物质NaCl为原料可以发展很多种工业,
(1)写出电解饱和食盐水的化学方程式______________________。
(2)以氯碱工业中的某些物质为原料制取漂白粉的化学方程式是_______________________
(3)从海水中获取的食盐中通常含有少量的MgCl2、Na2SO4等杂质,现采取下列方案将其提纯,其合理的操作顺序是__________________________________[来源:]
①取一定量的食盐晶体溶于水 ②加入过量的NaOH溶液 ③加入过量的BaCl2溶液
④过滤 ⑤蒸发溶液 ⑥加入过量的Na2CO3溶液 ⑦加入适量的盐酸,调节溶液的pH
Ⅱ:2007年11月18日凌晨乌克兰一煤矿因瓦斯爆炸而发生矿难,死亡人数超过100人;2007年12月12日,河南省某煤矿因发生煤矿瓦斯突发事故而导致12名矿工遇难.瓦斯是CH4和CO混合而成的有毒气体,遇到明火极易发生爆炸
(4)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比
(5)已知在101kPa时,CO的燃烧热为283kJ/mol,相同条件下若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,写出CH4完全燃烧的热化学方程式
120℃,101kPa下,a ml由CO、CH4组成的混合气体在bmlO2中完全燃烧后,恢复到原温度和压强
(6)若混合气体和O2恰好完全反应,产生bmlCO2,则混合气体中CH4的体积分数为
(7)若燃烧后气体体积缩小了a/4ml,写出a与b必须满足的关系式
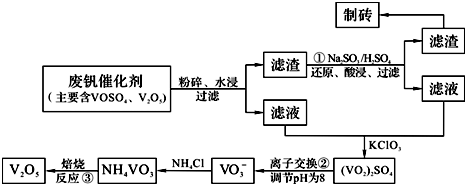
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
| ||
| ||
| 6 |
| 7 |
| n(SO3) |
| n(SO2) |





湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com