
题目列表(包括答案和解析)
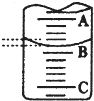 某化学实验小组探究市售食用白醋中醋酸的准确浓度,取25.00 mL某品牌食用白醋于锥形瓶中,在实验室用浓度为cb mol/L的标准NaOH溶液对其进行滴定.
某化学实验小组探究市售食用白醋中醋酸的准确浓度,取25.00 mL某品牌食用白醋于锥形瓶中,在实验室用浓度为cb mol/L的标准NaOH溶液对其进行滴定.| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
| (23.35+25.30)c |
| 2V |
| (23.35+25.30)c |
| 2V |
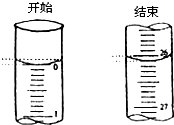 某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠 溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
⑴有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
⑵、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号 _____________
|
序号 |
锥形瓶中溶液 |
滴定管中溶液 |
选用指示剂 |
|
|
A |
碱 |
酸 |
石芯 |
(乙) |
|
B |
酸 |
碱 |
酚酞 |
(甲) |
|
C |
碱 |
酸 |
甲基橙 |
(甲) |
|
D |
酸 |
碱 |
酚酞 |
(乙) |
⑶、用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗碱式滴定管
⑷、已知滴定管中装有浓度为0.112mol/L的盐酸。逐滴加入到装有氢氧化钠的溶液的锥形瓶中。开始时读数及恰好反应时盐酸的读数见下表。
|
实验 编号 |
待测氢氧化钠溶液体积(mL) |
滴定开始读数(mL) |
滴定结束读数(mL) |
消耗盐酸体积(mL) |
|
① |
25.00 |
0.02 |
26.40 |
|
|
② |
25.00 |
0.04 |
25.81 |
|
|
③ |
25.00 |
0.03 |
25.78 |
|
|
④ |
25.00 |
0.20 |
25.96 |
|
试计算待测的氢氧化钠的物质的量浓度= .
Ⅰ.下图为常见仪器的部分结构(有的仪器被放大)
图A中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为n mL,仰视时读数为m mL,若m>n,则所使用的仪器是 (填字母标号)。
Ⅱ.某学生用标准0.25 mol·L—1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。 C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。 F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终? 。
④碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ,原因是 。
⑤假设操作均正确,标准液消耗了22.18mL,计算待测硫酸溶液的物质的量浓度(计算结果精确到小数点后二位) mol·L—1
Ⅲ.已知常温时醋酸的电离常数为1.8×10-5,一水合氨的电离常数为1.8×10-5。在少量Mg(OH)2悬浊液中,滴加适量饱和NH4Cl溶液,固体溶解。对于固体的溶解。
甲同学认为在氢氧化镁悬浊液中存在下列平衡:
Mg(OH)2 Mg2+ +2OH-
加入NH4Cl溶液,由于NH4+水解产生H+中和了Mg(OH)2电离产生的OH-而使平衡右移导致Mg(OH)2 溶解。
而乙同学却认为NH4Cl电离产生的NH4+结合了OH-生成了弱电解质NH3·H2O,使c(OH-)减小,平衡右移而导致Mg(OH)2 溶解。设计方案评价甲乙两位同学的观点:
_____________________________________ ______________________________
_________________________________________________________________________
Ⅰ.下图为常见仪器的部分结构(有的仪器被放大)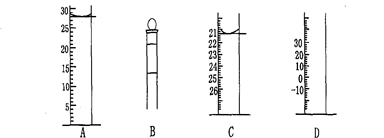
图A中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为n mL,仰视时读数为m mL,若m>n,则所使用的仪器是 (填字母标号)。
Ⅱ.某学生用标准0.25 mol·L—1 NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。 | |
| B.用待测定的溶液润洗酸式滴定管。 | C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |
 Mg2+ +2OH-
Mg2+ +2OH-1、B 2、D 3、B 4、C 5、D 6.D 7.D 8.A 9.B 10.A 11.A 12.B 13.D
14、C 15、ACD 16、B 17、C 18、A 19、D 20、A 21、CD
22. (1)C ; 0.600 ;(2)0.92;2.76;7.22;6.78(3)(1)BCE (2)4.3
23.

 2424.
2424.
24.解:当加速电压为U1时电子到达O点速度为
 ,则
,则 =
= ① (2分)
① (2分)
电子在偏转电场时有 ② (2分)
② (2分)
 ③(1分)
③(1分)
当加速电压为U2时电子到达O点速度为
 ,则
,则 ④(2分)
④(2分)
电子刚飞出偏转时偏移量: ⑤(2分)
⑤(2分)  ⑥(1分)
⑥(1分)
如图,由三角形相似有 ⑦ (4分)
⑦ (4分)
所以  (2分)
(2分)  (2分)
(2分)
25.(1)A与B第一次碰前: (2分)
(2分)
A与B第一次碰撞  (2分)
(2分)
 (2分)
(2分)
所以
 (2分)
(2分)
(2)B、C第一次碰撞  所以
所以 即B碰后停下 (2分)
即B碰后停下 (2分)
BC第一次碰前 (2分)
(2分)
此时 (2分)
(2分)
AB第一次碰后到第二次相碰前  (2分)
(2分)
所以 (2分)
(2分)
第二次相碰前 =
= (2分)
(2分)
W= (2分)
(2分)
26.(10分)
⑴ F Al (各2分) ⑵  (3分)
(3分)
⑶ 2Al + 2OH― + 2H2O=2AlO2― + 3H2↑(3分)
27.(20分)
⑴ C D(2分)
⑵ A D(2分)
⑶ 压强更高,所需动力更大,对材料的强度和设备的制造要求也更高。(2分)
⑷ 合成氨反应是可逆反应,实际消耗的N2(或H2)少于10 mol(或30 mol)(2分)
⑸①将注射器取下置于盛水的水槽中,若水进入注射器,气体体积减少,则说明有氨气生成。(2分)
② A B D(2分)
⑹①上述待测氨水 确保氨水的浓度不发生改变(各1分)
② 0.6250 mol/L(2分)
③ A C (1分)
⑺ N2 + 6e―=2N3―(2分)
28.(18分)
⑴  (各2分) ⑵ NaNH2 + NH4Cl=NaCl +
2NH3 (2分)
(各2分) ⑵ NaNH2 + NH4Cl=NaCl +
2NH3 (2分)
⑶ ①②(各2分)
⑷  (3分) ⑸ 4 (2分) ⑹ 1
(2分)
(3分) ⑸ 4 (2分) ⑹ 1
(2分)
⑺ C6H15N3 O 3 + NH3→C6H12N4 + 3H2O(2分)
29.(12分)
⑴ ①②④(2分)
⑵ 羧基 碳碳双键(各2分)
⑶ (CH3)2 CHCH
⑷(CH3)2 CHCH2 O H+ HC O O H→(CH3)3 CC O O H +H2 O(2分)
30.(22分)
⑴CO2(2分)
⑵B处O2多于D处,D处CO2多于B处(2分)
⑶减少(2分) 增加(2分) 上升(2分)
⑷装置中CO2量越来越少,暗反应下降,导致ATP和NADPH积累,进而使光反应下降。(2分) 乳酸(2分)
⑸15NH3→氨基酸及蛋白质(或含15N的有机物)(2分)根瘤菌、大豆(2分)脱氨基(2分)
肝脏(1分) 尿素(1分)
Ⅱ.(8分)
⑴细胞核(1分) 蒸馏水(1分) 不同浓度的NaCl溶液(1分)
⑵核糖体、线粒体(2分)
⑶胰岛素(1分)
 ⑷骨髓中的造血干细胞
抗体(2分)
⑷骨髓中的造血干细胞
抗体(2分)
⑸⑼答案见右图。(2分)注:①缺少细胞膜、中心体、纺锤体或染色体数目不符等错误均不得分。②姐妹染色体形态应一致,每一条染色体的“两臂”应“甩向”赤道板,否则不得分。右图的“美观性”不作要求。
31.(12分)
⑴①实验前要先测定甲、乙鼠的体温 ②实验要有重复性,仅用两只小白鼠进行实验有一定的偶然性。③增加丙组与甲鼠处理方法相同但不破坏下丘脑。
⑵赞同。先做不破坏下丘脑的实验,再做破坏下丘脑后的实验,进行自身前后对照(2分)
⑶BD AC (2分,缺一不给分)
⑷甲状腺激素和肾上腺素(2分,缺一不给分)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com