
题目列表(包括答案和解析)
有A、B、C、D、E、F六种原子序数依次增大的主族元素,其相关信息如下:
①短周期元素C原子的最外层有4个电子,E单质可在空气中燃烧;
②右表是元素周期表中的主族元素的一部分:
C | D | E |
|
| F |
③A、B为同周期相邻金属元素,A原子最外层电子数是其电子总数的1/6;
据些回答下列问题:
(1)D的元素符号是 ,F在元素周期表中的位置为 ;
(1)C的最高价氧化物与烧碱溶液反应的离子方程式为 ;
(3)B、E两元素分别形成的简单离子在水溶液中发生反应的离子方程式为 。
有A、B、C、D、E、F六种原子序数依次增大的主族元素,其相关信息如下:
①短周期元素C原子的最外层有4个电子,E单质可在空气中燃烧;
②上表是元素周期表中的主族元素的一部分;
③A、B为同周期相邻元素,A原子最外层电子数是其电子总数的1/6;
据此回答下列问题:
(1)D的元素符号是________,F在元素周期表中的位置为________;
(2)C的最高价氧化物与烧碱溶液反应的离子方程式为________;
(3)B、E两元素分别形成的简单离子在水溶液中反应的离子方程式为________.
| 1 | 4 |
 原子的该晶体中含有的共价键的数目为_________。
原子的该晶体中含有的共价键的数目为_________。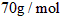 ,则该化合物的化学式为_________,其中可能含有的化学键类型为___________。已知该化合物在水中可以发生水解,其水解的离子方程式为_______________________。
,则该化合物的化学式为_________,其中可能含有的化学键类型为___________。已知该化合物在水中可以发生水解,其水解的离子方程式为_______________________。 (14分) 现有A、B、C、D、E、F六种原子序数依次增大的前四周期主族元素,且分属四个周期。A、E同主族;B、C、D为同周期相邻的三种元素;B元素形成的化合物种数是所有元素中最多的;D、E简单离子具有相同的电子层结构;F与B可形成![]() 型离子化合物。请填写下列空白:
型离子化合物。请填写下列空白:
(1)D与E按原子个数比![]() 形成的化合物的电子式为 。
形成的化合物的电子式为 。
(2)B可形成多种同素异形体,其中一种同素异形体熔、沸点很高,硬度大,该同素异形体的晶体类型为 ,含有![]() 原子的该晶体中含有的共价键的数目为 。
原子的该晶体中含有的共价键的数目为 。
(3)由A、B、D、F四种元素组成的化合物与过量的E的最高价氧化物对应水化物反应的离子方程式为 。
(4)C与E形成的―种化合物中,E元素的质量分数为35.4%,该化合物的摩尔质量不超过![]() ,则该化合物的化学式为 ,其中可能含有的化学键类型为 。已知该化合物在水中可以发生水解,其水解的离子方程式为 。
,则该化合物的化学式为 ,其中可能含有的化学键类型为 。已知该化合物在水中可以发生水解,其水解的离子方程式为 。
一、选择题(每小题2.5分,共50分)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
D
B
D
C
D
B
A
B
C
题号
11
12
13
14
15
16
17
18
19
20
答案
C
C
D
C
A
D
C
B
C
A
二、填空题(每空2分,共28分)
21、(1)AlO2-;(2)Zn+2OH-=ZnO22-+H2↑ (3)①③④
22、(1)Fe3++3H2O Fe(OH)3+3H+ CaCO3+2H+===Ca2++CO2↑+H2O
Fe(OH)3+3H+ CaCO3+2H+===Ca2++CO2↑+H2O
(2)C
(3)HI是强电解质,使胶体聚沉;2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O
(4)①Fe(OH)3, 0.06mol;②0<X≤0.6
23.(1)P,第四周期第ⅥA族;
(2)SiO2+2OH-===SiO32-+H2O;
(3)2Al3++3S2-+6H2O===2Al(OH)3↓+3H2S↑
三、实验题(每空2分,共20分)
24.(1)2、5、1、2、5、3 (2)0.2000;(3)ACD
25.(1)Cu2O或Fe2O3和Cu2O的混合物;
(2)取少许红色粉末溶于足量稀硫酸中,充分溶解后滴加KSCN溶液,再滴加双氧水;
有红色固体生成,加KSCN溶液不显红色,再加双氧水后显红色。
(3)①双氧水、碱式碳酸铜;②Fe(OH)3;③蒸发、浓缩、冷却、结晶。
四、计算题(10分)
26.(1)NH4+、Al3+、SO42-( (3分)
(2)NH4Al(SO4)2?12H2O[或(NH4)2SO4?Al2(SO4)3?24H2O] (4分)
 (3)
(3)
(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com