
题目列表(包括答案和解析)
(10分)碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
W(s)+ I2(g) WI2(g)ΔH<0
为模拟上述反应,在450℃时向一体积为2L的恒容密闭容器中加入0.1mol碘单质和足量的钨,2min后反应达到平衡,测得碘蒸气浓度为0.005 mol·L-1。请回答下列问题:
(1)前两分钟内碘蒸气的反应速率为 ▲ 。
(2)能够说明上述反应已经达到平衡状态的有 ▲ 。
A.I2与WI2的浓度相等
B.容器内气体压强不再变化
C.W的质量不再变化
D.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等
E.容器内混合气体的密度保持不变
(3)下图为该反应在450℃时的时间—速率图,则t2时刻改变的外界条件可能是 ▲ ,若t4时刻将容器压缩至一半(各物质状态不变),保持该条件至t6,请在图中画出t4到t6时间段内大致曲线图,并在相应曲线上标上υ3(正)、υ3(逆)
t0 t1 t2 t3 t4 t5 t6 t
(4)假设灯丝温度为660℃,灯泡壁温度为350℃。请根据化学反应原理分析在灯泡内充入碘能够延长钨丝寿命的原因 ▲ 。
(10分)碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
W(s)+ I2(g)
 WI2(g)ΔH<0
WI2(g)ΔH<0
为模拟上述反应,在450℃时向一体积为2L的恒容密闭容器中加入0.1mol碘单质和足量的钨,2min后反应达到平衡,测得碘蒸气浓度为0.005 mol·L-1。请回答下列问题:
(1)前两分钟内碘蒸气的反应速率为 ▲ 。
(2)能够说明上述反应已经达到平衡状态的有 ▲ 。
A.I2与WI2的浓度相等
B.容器内气体压强不再变化
C.W的质量不再变化
D.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等
E.容器内混合气体的密度保持不变
(3)下图为该反应在450℃时的时间—速率图,则t2时刻改变的外界条件可能是 ▲ ,若t4时刻将容器压缩至一半(各物质状态不变),保持该条件至t6,请在图中画出t4到t6时间段内大致曲线图,并在相应曲线上标上υ3(正)、υ3(逆)
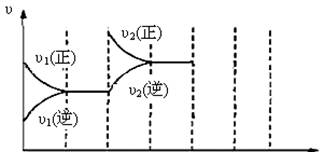
t0 t1 t2 t3 t4 t5 t6 t
(4)假设灯丝温度为660℃,灯泡壁温度为350℃。请根据化学反应原理分析在灯泡内充入碘能够延长钨丝寿命的原因 ▲ 。
碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
W(s)+ I2(g) ![]() WI2(g)ΔH<0
WI2(g)ΔH<0
为模拟上述反应,在450℃时向一体积为2L的恒容密闭容器中加入0.1mol碘单质和足量的钨,2min后反应达到平衡,测得碘蒸气浓度为0.005 mol·L-1。请回答下列问题:
(1)前两分钟内碘蒸气的反应速率为 ▲ 。
(2)能够说明上述反应已经达到平衡状态的有 ▲ 。
A.I2与WI2的浓度相等
B.容器内气体压强不再变化
C.W的质量不再变化
D.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等
E.容器内混合气体的密度保持不变
(3)下图为该反应在450℃时的时间—速率图,则t2时刻改变的外界条件可能是 ▲ ,若t4时刻将容器压缩至一半(各物质状态不变),保持该条件至t6,请在图中画出t4到t6时间段内大致曲线图,并在相应曲线上标上υ3(正)、υ3(逆)
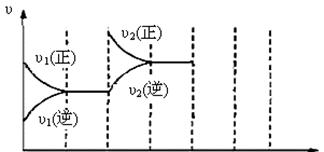 |
t0 t1 t2 t3 t4 t5 t6 t
(4)假设灯丝温度为660℃,灯泡壁温度为350℃。请根据化学反应原理分析在灯泡内充入碘能够延长钨丝寿命的原因 ▲ 。

水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H = +131.3 kJ•mol-1
CO (g) +H2 (g) △H = +131.3 kJ•mol-1
(1)该反应的平衡常数K随温度的升高而___________(增大 / 减小 / 不变)。
 (2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
(2)上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后正反应速率(ν正)随时间的变化:
① 缩小容器体积(用实线表示)
② 降低温度(用虚线表示)
(3)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ________ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正____ν逆 |
(4)己知:2C (s) + O2(g) = 2CO (g) △H = -221.0 kJ·mo1-1
2CO(g) + O2(g) = 2CO2 (g) △H = -566.0 kJ·mo1-1
2H2 (g) + O2 (g) = 2H2O (g) △H = -483.6 kJ·mo1-1
若将24g炭完全转化为水煤气,然后再充分燃烧,整个过程的焓变为△H = kJ/mol。
生物部分:1.A 2.C 3. D 4.C 5.D
30.(1)a应增加两组小白鼠的数量,避免偶然因素导致实验结果不准确甚至实验失败
b甲乙两组小白鼠的健康和生理状况应该一致
c实验前应先测定甲乙两组小白鼠的体温
d甲乙两组小白鼠应置于相同的较低温度(比如
(2)甲状腺激素和肾上腺素 神经??体液
(3)①神经系统兴奋性降低,精神萎靡 ②影响甲状腺激素的分泌,食欲减低 ③影响抗利尿激素的合成,尿量增加(任选两项,其它合理答案酌情给分)
(4)
测量次数(间隔4小时)
1
2
3
4
5
6
7
甲组鼠平均体温
乙组鼠平均体温
31.(1)正交、反交
(2)细胞质遗传 ①为母系遗传,②具有相对性状的亲本杂交,后代性状没有一定的分离比
(3)①细胞核遗传 ②如下图。
P: ♀DD × dd♂
右旋螺 ↓ 左旋螺
F1 Dd
右旋螺
↓自交
F2 1/4DD 2/4Dd l/4dd
右旋螺 右旋螺 右旋螺
↓自交 ↓自交 ↓自交
F3 1/4DD 2/4(1/4DD、2/4Dd、l/4dd) l/4dd
右旋螺(表现为母体基因型) 左旋螺
3 : 1
化学部分:6.B 7.D 8.A 9D
26.(12分)
(1)漏斗、玻璃棒 (2分) ;
(2)蒸发浓缩、冷却结晶 (2分)
(3)Cu+H2O2+H2SO4+3H2O=CuSO4?5H2O
(或Cu+H2O2+H2SO4=CuSO4+2H2O) (3分)
(4)途径Ⅱ(1分);滤液A是NaAlO2和NaOH溶液,途径Ⅰ直接向A中加入盐酸得到的AlCl3溶液中含大量NaCl杂质;途径Ⅱ通入CO2气体得到Al(OH)3沉淀,将Al(OH)3恰好溶解于盐酸中得到的是纯净的AlCl3溶液 (4分)
27.(16分)
 (1)C4H8O2 (2分) (2)3 (1分) (3)消去反应(1分)
(1)C4H8O2 (2分) (2)3 (1分) (3)消去反应(1分)

(5)
 |
28.(16分)
(1)c(1分)
(2)①(Ⅰ)饱和碳酸氢钠溶液;(1分)除去CO2中的HCl气体(1分)
(Ⅱ)吸收未反应完的NH3(1分)(答“防止倒吸”或“吸收CO2”不给分);
(Ⅲ)过滤(1分) 玻璃棒、漏斗、烧杯(3分)
②(Ⅰ)氨气极易溶解于水,能形成较大浓度的溶液,有利于二氧化碳吸收,生成更多的碳酸氢铵。(共2分)
(Ⅱ)增大气体与溶液接触面积,提高CO2的吸收率。(2分)
(3)83.6%(或0.863)(0.86也得分)(2分)
(4)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2;往饱和Na2CO3溶液中通入过量CO2等。其他合理方法均可;化学方程式也可。)(2分)
29.(16分)
(1)减小(2分)
(2)BC(2分)(只答一个且正确的给1分,错选1个0分)
(3)①b;②f(各3分)
(4)(6分)①0.60 ②>
物理部分:14.A 15.D 16.AB 17.A 18.B 19.C 20.B 21.BD
22.(1)(6分)
(2)(12分)(a)③ ② ⑤ ⑥(每空1分)
(b)二组(2分) (c)
 (每空3分)
(每空3分)
23.(15分)
(1)风突然停止,船体只受水的阻力f做减速运动,船体加速度大小 ,船只受水的阻力
,船只受水的阻力
(2)在单位时间内,对吹入帆船的空气(柱)应用动量定理.

 ∴
∴
24.(19分)
(1)在圆形磁场压内 ∴
∴ (6分)
(6分)
(2)粒子不从O3射出的条件
 ①
①
 ② (6分)
② (6分)
(3)导体棒匀速运动时,速度为
则 ∴
∴
则动量守恒 (7分)
(7分)
25.(20分)
(1) ∴
∴
(2)由功解关系得
 ∴
∴
两球碰后结合为C,C物之速v1 

(3)电场变化后 因 (向上)
(向上)
向下向心力  ∴
∴
不能作圆运动,而从底点作类平抛运动,经时间t,设在Q点绷紧.

 可得
可得
 故绳绷紧恰于水平位置,水平方向速度变为0,以竖直方向
故绳绷紧恰于水平位置,水平方向速度变为0,以竖直方向 作圆周运动,最高点速度设为
作圆周运动,最高点速度设为
 ∴
∴
 ∴
∴
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com