
题目列表(包括答案和解析)
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。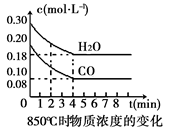
(1)CO和H2O浓度变化如上图,则在该温度下,该反应的平衡常数K= 。
0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,
容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2
(g) △H<0。
CO2(g) +H2
(g) △H<0。
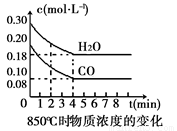
(1)CO和H2O浓度变化如上图,则在该温度下,该反应的平衡常数K= 。
0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,
容器内各物质的浓度变化如下表。
|
时间(min) |
CO |
H2O |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
①表中3min~4min之间反应处于_________状态; c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
 CO(g) +H2O(g)
CO(g) +H2O(g) ![]() CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。
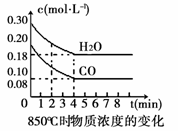
(1)CO和H2O浓度变化如右图,则在该温度下,该反应
的平衡常数K= 。
0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,
容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min~4min之间反应处于_________状态; c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0.200 | 0.300 | |||
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
| |||||||||||||||||||||||||||||||||
一、选择题
1.C 2.D 3.A 4.D 5.C 6.C 7.D 8.C 9.D 10.D
11.A 12.B 13.B二、选择题
14.D 15.D 16.AC 17.AD 18.D 19.C 20.CD 21.A
三、选择题
22.(18分)
(1)(每空3分)24.12~24.14 0.514~0.517
(2)(每空4分)偏小; 理科综合.files/image226.gif)
(3)(每空4分)图略
(4)A.轨迹图略(任意画出理科综合.files/image150.gif) 点不给分)
点不给分)
B.参考方法一:在轨迹上选两个点A、B
如图1,量出理科综合.files/image229.gif) 、
、理科综合.files/image231.gif) 、
、理科综合.files/image233.gif)
推导:理科综合.files/image235.gif)
理科综合.files/image237.gif)
理科综合.files/image239.gif)
导出 理科综合.files/image241.gif)
理科综合.files/image243.jpg)
参考方法二:在轨迹上选三个点A、B、C
如图2,量出理科综合.files/image245.gif) 、
、理科综合.files/image247.gif) 、
、理科综合.files/image249.gif)
推导 理科综合.files/image251.gif)
导出 理科综合.files/image253.gif)
理科综合.files/image255.jpg)
其他方法:根据抛物线方程推导等(略)
23.(15分)解:(1)设最高点
理科综合.files/image257.gif) (2分)
(2分)
最低点理科综合.files/image259.gif) (2分)
(2分)
机械能守恒理科综合.files/image261.gif) (2分)
(2分)
理科综合.files/image263.gif) (2分)
(2分)
理科综合.files/image265.gif) (2分)
(2分)
(2)理科综合.files/image267.gif) (3分)
(3分)
所以理科综合.files/image269.gif) (2分)
(2分)
24.(19分)解:(1)理科综合.files/image182.gif) 作用后,
作用后,理科综合.files/image272.gif) 均做匀加速直线运动
均做匀加速直线运动
理科综合.files/image274.gif)
理科综合.files/image276.gif) (1分)
(1分)
理科综合.files/image278.gif)
理科综合.files/image280.gif) (1分)
(1分)
理科综合.files/image282.gif) (1分)
(1分)
设经理科综合.files/image284.gif) 时间
时间理科综合.files/image168.gif) 、
、理科综合.files/image170.gif) 相遇,相遇时
相遇,相遇时理科综合.files/image288.gif) (1分)
(1分)
理科综合.files/image290.gif) (1分)
(1分)理科综合.files/image292.gif) 解得
解得理科综合.files/image294.gif) (1分)
(1分)
(2)相遇前理科综合.files/image296.gif) (1分)
(1分)
理科综合.files/image298.gif) (1分)
(1分)
理科综合.files/image300.gif) (1分)
(1分)
最终理科综合.files/image272.gif) 相对静止,
相对静止,理科综合.files/image182.gif) 撤去后系统
撤去后系统理科综合.files/image304.gif)
理科综合.files/image306.gif) (1分)
(1分)
理科综合.files/image308.gif)
(3)理科综合.files/image292.gif) (1分)
(1分)
理科综合.files/image311.gif) (1分)
(1分)
理科综合.files/image313.gif) (1分)
(1分) 理科综合.files/image315.gif) (1分)
(1分)
理科综合.files/image317.gif) (1分)
(1分) 理科综合.files/image319.gif) (1分)
(1分)
理科综合.files/image321.gif) (1分)
(1分)
理科综合.files/image323.gif) (1分)
(1分)
理科综合.files/image325.gif) (1分)
(1分)
25.(20分)(1)由理科综合.files/image327.gif) 得
得理科综合.files/image329.gif) (3分)
(3分)
由理科综合.files/image331.gif) (
(理科综合.files/image092.gif) 为电子圆轨道半径) (3分)
为电子圆轨道半径) (3分)
得理科综合.files/image334.gif) (3分)
(3分)
(3分)
理科综合.files/image336.jpg)
(2)由图可知:理科综合.files/image338.gif) (3分)
(3分)
圆轨道对应的弦越长,圆心角越大,即偏转角越大。当弦长为圆形磁场的直径时.电子射出磁场区域时的偏转角最大为理科综合.files/image340.gif) (3分)
(3分)
由图可知:理科综合.files/image342.gif) (2分)
(2分)
26.(15分)(每空3分共15分)A BaCl2 B(NH4)2 SO4
C AgNO3 D NaCO3 E A12(SO4)3
27.(20分)(Ⅰ)(共14分)
(1)18(2分)
(2)CH2O2(2分) HCOOH(2分)
(3)C2 H2O3(2分) OHC―COOH(2分)
(4)CH3COOH(2分) HCOOCH3(2分)
(Ⅱ)(6分)理科综合.files/image344.jpg)
理科综合.files/image346.jpg) (每空2分)
(每空2分)
28.(13分)
(1)A12O3(2分)Fe2O3(2分)
(2)2Al+Fe2O3====Al2O3+2Fe(3分)
(3)Al理科综合.files/image017.gif) +3A1O
+3A1O理科综合.files/image025.gif) +4H2O====4Al<OH>3↓(3分 )
+4H2O====4Al<OH>3↓(3分 )
(4)理科综合.files/image350.gif) (3分)
(3分)
29.(12分)
(1)C→B→D→A→G→H→E→F(4分)
(2)使漏斗下端管口紧靠烧杯内壁;及时关闭活塞,不要让上层液体流出 (2分)
使漏斗内外空气相通,以保证进行(E)操作时漏斗里液体能够流出 (2分)
(3)CCl4与水不互溶l而且溴在CCl4中的溶解度比在水中的大很多(2分)
(4)(A)(C)(2分)
30.(22分)I.(8分)(每空1分)
① 生长素促进植物生长具有双重性,双子叶植物比单子叶植物对生长素敏感
② b a ③ D
Ⅱ.(14分)① 竞争(1分) 种类斗争、寄生、捕食等(3分)
② 食物和栖息场所(2分)
③ 自动调节(1分);
④ 以甲种群植物为食的其他生物也随之减少,甚至灭绝(2分)
⑤ 缺乏有利变异(2分)l
⑥ 样方法(1分);
⑦ 衰退型 增长型(2分)
31.(20分)
(1)基因突变(2分);① 一种氨基酸可以由多个密码子决定(2分);
② 突变发生在基因中的非编码序列(2分)(只答非编码区或内含子中的一个给1分)
(2)解离→漂洗→染色→制片(2分);染色体数(2分)
结果预测和分析:
① A装片细胞中的染色体数与甲装片细胞中的染色体数相等一A植株为品种乙(2分);
② A装片中细胞中染色体数是甲装片细胞中染色体数的两倍一A植株为品种丙(2分);
(3)方法1:用植株A与品种甲的植株杂交,获得F1;再用F1自交;观察F1是否结果实。
方法2:用A植株的花药进行离体培养,获得单倍体;再用单倍体植株杂交;观察单倍体植株是否结果实。(3分)(答出一种方案即可。其他合理答案酌情给分。)
(4)人工合成(或反转录法等)(1分);真核生物的基因含有不表达的内含子(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com