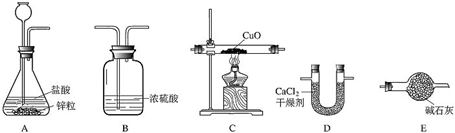
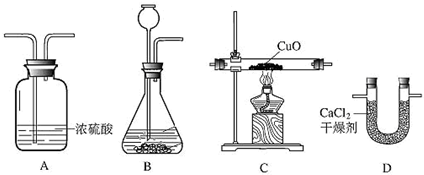
利用干燥而纯净的氢气还原灼热氧化铜的实验测定水的质量组成,其装置如图所示.反应后其实验测定的数据如下表所列.
|
实验前 |
实验后 |
| (氧化铜+玻璃管)的质量/g |
150.5 |
144.1 |
| (氯化钙+U型管)的重量/g |
210.8 |
218.2 |
试回答:
(1)装置B中金属和酸反应制取氢气,最好选择下列哪一组
B
B
.
A、铜和浓硫酸 B、锌和稀硫酸 C、镁和浓盐酸 D、铁和稀硝酸
(2)装置正确的连接顺序(自左向右)是(填字母)
B、A、C、D
B、A、C、D
.
(3)装置A的作用是
除去氢气中混有的水蒸汽
除去氢气中混有的水蒸汽
.
(4)根据实验数据计算填空:
水中氢、氧两元素的质量比为
5:32
5:32
.(化成最简整数比)
(5)本次实验测定的结果和理论上水中氢、氧两元素的质量比相比较是(填“偏高”、“偏低”或“恰好相符”)
偏高
偏高
,导致这样结果的原因可能是
A、B、C、D、E
A、B、C、D、E
(填字母).
A、装置C开始加热的时候没有用氢气赶尽装置中的空气
B、实验前装置D称量后再连接然后开始实验导致的必然结果
C、实验后称量装置D的质量时动作太慢,吸收了空气中的水蒸汽
D、托盘天平的精确度不高,有误差
E、实验后没有继续通入氢气直到冷却,就开始称量装置D的质量,
导致热铜与空气中的氧气反应
F、氧化铜没有完全反应,反应后装置C中还有氧化铜
(6)依据(5)的结论回答问题
用锌、氧化铜、稀硫酸为原料制取单质铜,有下列两种途径:
(1)Zn
H
2 Cu
(2)CuO
CuSO
4Cu
当实验室用这两种途径制得相同质量的铜时,下列叙述符合实际实验结果的是(
A
A
)
A、消耗相同质量的氧化铜 B、消耗相同质量的锌
C、消耗相同质量的硫酸 D、生成硫酸锌的质量可能相同.