在用稀盐酸和氢氧化钠溶液研究中和反应实验时,某化学兴趣小组认真观察、详实记录,进行了一些探究活动.请完成下列问题:
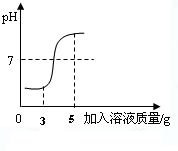
(1)小明同学利用“pH计”测定并绘制了溶液的酸碱度变化如图所示.
①化学方程式为
HCl+NaOH═NaCl+H2O
HCl+NaOH═NaCl+H2O
.
②根据图示可知:小明的实验是用胶头滴管逐滴将
稀盐酸
稀盐酸
(选填“稀盐酸”或“氢氧化钠溶液”)滴加另一种溶液中.
③在加入溶液的质量至5g时,所得溶液中溶质的化学式为
NaCl、NaOH
NaCl、NaOH
.
(2)细心的小华同学观察非常仔细,在实验进行几秒钟之后,发现溶液中有少量气泡产生.经过小组讨论,他们一致认为NaOH溶液在空气中变质了,依据是
稀盐酸与NaOH反应无明显现象,只能与NaOH变质后生成的Na2CO3反应产生气泡
稀盐酸与NaOH反应无明显现象,只能与NaOH变质后生成的Na2CO3反应产生气泡
.
为此,他们还进一步设计了两个检验NaOH溶液是否变质的实验方案来重复验证:
方案一:取少量溶液样品,滴入BaCl
2溶液,若有白色沉淀生成,则证明NaOH溶液变质了.
方案二:取一定量溶液样品,滴加适量酚酞溶液,若溶液变红,则证明NaOH溶液变质了.
你不同意上述两个实验方案中的哪一个?简述你的理由.
因为NaOH和NaOH变质后生成的溶液都显碱性,都能使无色酚酞试液变红色,不能用来判断NaOH溶液是否变质
因为NaOH和NaOH变质后生成的溶液都显碱性,都能使无色酚酞试液变红色,不能用来判断NaOH溶液是否变质
.


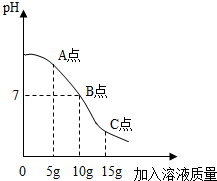 (2013?历城区一模)在用稀盐酸和氢氧化钠溶液研究中和反应实验时,某化学兴趣小组认真观察、详实记录,进行了一些探究活动.请完成下列问题:
(2013?历城区一模)在用稀盐酸和氢氧化钠溶液研究中和反应实验时,某化学兴趣小组认真观察、详实记录,进行了一些探究活动.请完成下列问题: