被称为“绿色氧化剂”的过氧化氢(H
2O
2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO
2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:
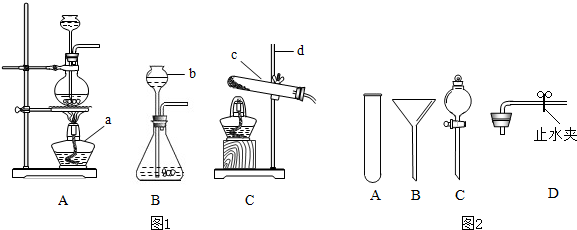
(1)写出图1中标号仪器的名称:
a、
酒精灯
酒精灯
;b、
长颈漏斗
长颈漏斗
;
c、
试管
试管
;d、
铁架台
铁架台
;
(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置?
B
B
(填序号),主要理由是
过氧化氢在常温下(不需要加热)可以分解生成氧气
过氧化氢在常温下(不需要加热)可以分解生成氧气
.
(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从如图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是
C
C
(填序号),它更换原装置的
b
b
.控制反应速度的原理是:
分液漏斗可以使液体的滴加随开随停
分液漏斗可以使液体的滴加随开随停
.
(4)天然气、沼气的主要成分是甲烷(CH
4),它是无色无味的气体,密比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体. 若用此法制取甲烷气体,其气体发生装置选择
C
C
(从图1A、B、C中选择),可采用
向下排空气法
向下排空气法
或
排水法
排水法
收集.




 被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:
被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:



