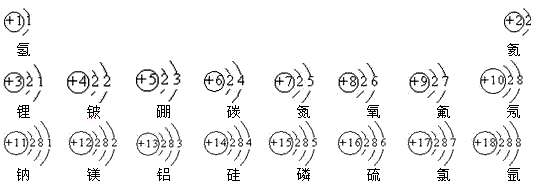
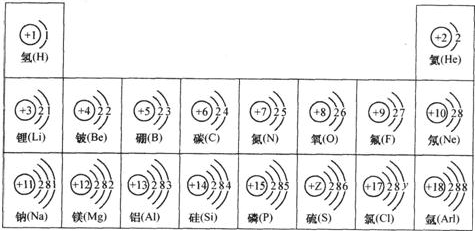
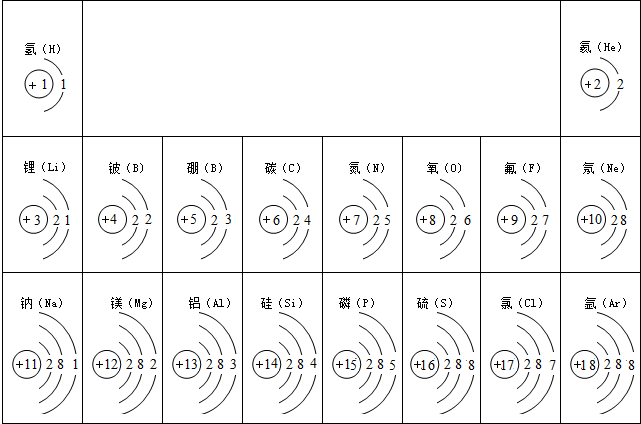
元素周期表是化学学习的重要工具,依据下表回答问题:
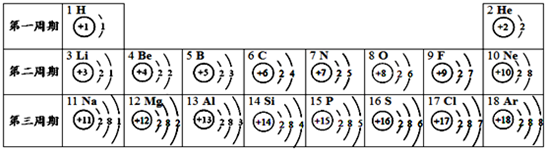
(1)表中9号元素属于
非金属
非金属
(填“金属”或“非金属”)元素,在化学反应中易
得到
得到
(填“失去”或“得到”)电子,形成
F-
F-
(填化学符号).
(2)氮化镁的化学式为
Mg3N2
Mg3N2
.
(3)He、Ne、Ar分别位于每一周期最后的原因是
原子的最外层电子均达到了稳定结构(或都属于稀有气体的原子)
原子的最外层电子均达到了稳定结构(或都属于稀有气体的原子)
.
(4)F、Cl、S三种非金属元素的原子得电子能力逐渐减弱,我能根据这三种非金属元素的原子结构推测:非金属元素的原子得电子能力的强弱主要与
最外层电子数
最外层电子数
有关(任填一点合理答案即可).