
题目列表(包括答案和解析)
小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
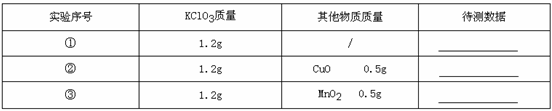
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g | |
小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。

(1)上述实验应测量的“待测数据"是_________;
(2)若实验②比实验①的“待测数据”更___________(选填“大"或“小"),说明氧化铜能加快氯酸钾的分解速率;
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,说明
________________;
(4)再将该黑色粉末放入试管中,加入________________,若观察到_______,说明黑色粉末的化学性质在反应前后保持不变。
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是_________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com