
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
Ҫ«Т»¶ЁБҝxFeSO4ЎӨy(NH4)2SO4ЎӨ6H2Oҫ§МејУИлөҪ№эБҝNaOHИЬТәЦРЈ¬јУИИЙъіЙNH30.85 g(јЩИзЙъіЙNH3өДИ«ІҝТЭіц)Ј¬№эВЛЎўПҙөУЎўЧЖЙХЈ¬өГFe2O3№ММе2.0 gЈ®ФтxЈ¬yөД№ШПөХэИ·өДКЗ
AЈ®xЎГyЈҪ1ЎГ1
BЈ®xЎГyЈҪ1ЎГ2
CЈ®xЎГyЈҪ1ЎГ4
DЈ®xЎГyЈҪ2ЎГ1


 x Fe + y H2OЈ¬Fe3C + 2H2
x Fe + y H2OЈ¬Fe3C + 2H2 3 Fe + CH4ЎЈ
3 Fe + CH4ЎЈ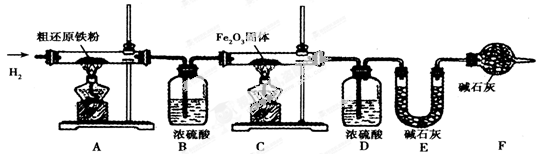
 3 CO2 + 6H2O + 8 FeЈЁјЩЙиГҝІҪ·ҙУҰ¶јНкИ«Ј¬ЗТІ»ҝјВЗЧ°ЦГДЪФӯУРҝХЖш¶ФІв¶ЁҪб№ыөДУ°ПмЈ©ЎЈ
3 CO2 + 6H2O + 8 FeЈЁјЩЙиГҝІҪ·ҙУҰ¶јНкИ«Ј¬ЗТІ»ҝјВЗЧ°ЦГДЪФӯУРҝХЖш¶ФІв¶ЁҪб№ыөДУ°ПмЈ©ЎЈ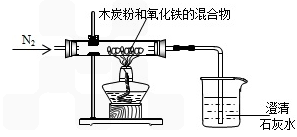
ТСЦӘДҫМҝ·Ы(јЩЙиДҫМҝ·ЫЦРІ»ә¬ЖдЛыФУЦК)әНFe2O3Ј¬ФЪјУИИМхјюПВ·ўЙъ»ҜС§·ҙУҰЈ¬РЛИӨРЎЧйН¬С§¶ФёГКөСйҪшРРИзПВМҪҫҝЎЈ Ј®
I ЙъіЙ№ММеЧйіЙ·ЦОц
(1)КөСй№эіМЦРҝЙТФ№ЫІмөҪУРәЪЙ«№ММеЙъіЙЈ¬РЎББИПОӘЙъіЙБЛМъ·ЫЈ¬ө«РЎБйИҙУРІ»Н¬ҝҙ·ЁЈ¬АнУЙКЗ ЎЈ
(2)ОӘҪшТ»ІҪИ·¶ЁәЪЙ«№ММеіЙ·ЦЈ¬РЎ»¶Ҫ«ЙъіЙөД№ММеИЬУЪЧгБҝПЎБтЛбЈ¬·ўПЦУРҙуБҝЖшЕЭІъЙъЈ¬ИфН¬КұіцПЦ өДПЦПуЈ¬ФтЙъіЙөДәЪЙ«№ММеИ«ІҝКЗМъЎЈ
ўт ЙъіЙЖшМеіЙ·Ц·ЦОц
ЎҫМбіцјЩЙиЎҝЙъіЙЖшМеөДҝЙДЬЧйіЙУРИэЦЦЈә
јЩЙи1ЈәЙъіЙЖшМеКЗ¶юСх»ҜМјЈ»
јЩЙи2ЈәЙъіЙЖшМеКЗТ»Сх»ҜМјЈ»
јЩЙи3ЈәЙъіЙЖшМеКЗ ЎЈ
ЎҫЙијЖКөСйЎҝОӘИ·¶ЁЙъіЙЖшМеөДЧйіЙЈ¬РЎЧйН¬С§ЙијЖКөСйЧ°ЦГИзНјЎЈ
(1)КөСйЦРНЁИлөДЖшМеКЗҙҝҫ»ёЙФпөДN2Ј¬·ЦОцІ»НЁИлҝХЖшөДЦчТӘАнУЙКЗ ЈЁМоРтәЕЈ©ЎЈ
AЈ®ҝХЖшЦРөД¶юСх»ҜМј»бК№КҜ»ТЛ®ұд»лЧЗ
BЈ®ҝХЖшЦРөДСхЖш»бәНДҫМҝ·Ы·ҙУҰЙъіЙCO»тCO2¶шёЙИЕКөСйҪб№ы
CЈ®ҝХЖшЦРөД¶юСх»ҜМјЎўЛ®ХфЖш»бәНДҫМҝ·Ы·ҙУҰЙъіЙCO¶шёЙИЕКөСйҪб№ы
(2)¶ЁРФСРҫҝЈәИфКөСй№эіМЦРҝЙТФ№ЫІмөҪіОЗеКҜ»ТЛ®ұд»лЧЗЈ¬ФтЦӨГч·ҙУҰЙъіЙөДЖшМеЦР
Т»¶Ёә¬УР ЎЈ
(3)¶ЁБҝСРҫҝЈәПЦЧјИ·іЖИЎ16.0 gСх»ҜМъУл2.4 gДҫМҝ·Ы»мәПЈ¬ФЪЙПКцЧ°ЦГЦРНкИ«·ҙУҰЎЈІвөГКЈУа№ММеЦКБҝОӘ11.2 gЈ¬ЗТДЬНкИ«ИЬУЪПЎСОЛбЎЈ
ЎҫКөСйҪбВЫЎҝҙҰАнЙПКцКөСйКэҫЭәуҝЙЦӘЈ¬јЩЙи ХэИ·ЎЈ

(6·Ц)ТСЦӘДҫМҝ·Ы(јЩЙиДҫМҝ·ЫЦРІ»ә¬ЖдЛыФУЦК)әНFe2O3Ј¬ФЪјУИИМхјюПВ·ўЙъ»ҜС§·ҙУҰЈ¬РЛИӨРЎЧйН¬С§¶ФёГКөСйҪшРРИзПВМҪҫҝЎЈ
I ЙъіЙ№ММеЧйіЙ·ЦОц
(1)КөСй№эіМЦРҝЙТФ№ЫІмөҪУРәЪЙ«№ММеЙъіЙЈ¬РЎББИПОӘЙъіЙБЛМъ·ЫЈ¬ө«РЎБйИҙУРІ»Н¬ҝҙ·ЁЈ¬АнУЙКЗ ЎЈ
(2)ОӘҪшТ»ІҪИ·¶ЁәЪЙ«№ММеіЙ·ЦЈ¬РЎ»¶Ҫ«ЙъіЙөД№ММеИЬУЪЧгБҝПЎБтЛбЈ¬·ўПЦУРҙуБҝЖшЕЭІъЙъЈ¬ИфН¬КұіцПЦ өДПЦПуЈ¬ФтЙъіЙөДәЪЙ«№ММеИ«ІҝКЗМъЎЈ
ўт ЙъіЙЖшМеіЙ·Ц·ЦОц
ЎҫМбіцјЩЙиЎҝЙъіЙЖшМеөДҝЙДЬЧйіЙУРИэЦЦЈә
јЩЙи1ЈәЙъіЙЖшМеКЗ¶юСх»ҜМјЈ»
јЩЙи2ЈәЙъіЙЖшМеКЗТ»Сх»ҜМјЈ»
јЩЙи3ЈәЙъіЙЖшМеКЗ ЎЈ
ЎҫЙијЖКөСйЎҝОӘИ·¶ЁЙъіЙЖшМеөДЧйіЙЈ¬РЎЧйН¬С§ЙијЖКөСйЧ°ЦГИзНјЎЈ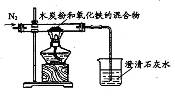
(1)КөСйЦРНЁИлөДЖшМеКЗҙҝҫ»ёЙФпөДN2Ј¬·ЦОцІ»НЁИлҝХЖшөДЦчТӘАнУЙКЗ ЈЁМоРтәЕЈ©ЎЈ
AЈ®ҝХЖшЦРөД¶юСх»ҜМј»бК№КҜ»ТЛ®ұд»лЧЗ
BЈ®ҝХЖшЦРөДСхЖш»бәНДҫМҝ·Ы·ҙУҰЙъіЙCO»тCO2¶шёЙИЕКөСйҪб№ы
CЈ®ҝХЖшЦРөД¶юСх»ҜМјЎўЛ®ХфЖш»бәНДҫМҝ·Ы·ҙУҰЙъіЙCO¶шёЙИЕКөСйҪб№ы
(2)¶ЁРФСРҫҝЈәИфКөСй№эіМЦРҝЙТФ№ЫІмөҪіОЗеКҜ»ТЛ®ұд»лЧЗЈ¬ФтЦӨГч·ҙУҰЙъіЙөДЖшМеЦРТ»¶Ёә¬УР ЎЈ
(3)¶ЁБҝСРҫҝЈәПЦЧјИ·іЖИЎ16.0 gСх»ҜМъУл2.4 gДҫМҝ·Ы»мәПЈ¬ФЪЙПКцЧ°ЦГЦРНкИ«·ҙУҰЎЈІвөГКЈУа№ММеЦКБҝОӘ11.2 gЈ¬ЗТДЬНкИ«ИЬУЪПЎСОЛбЎЈ
ЎҫКөСйҪбВЫЎҝҙҰАнЙПКцКөСйКэҫЭәуҝЙЦӘЈ¬јЩЙи ХэИ·ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com