
题目列表(包括答案和解析)
| ||
| ||
化学与环境和人们的生活密切相关。某校化学兴趣小组从摄影店收集到一些废弃的定影液(主要成分为![]() 和
和![]() ) ,并对定影液进行处理,回收金属银和硝酸锌固体。
) ,并对定影液进行处理,回收金属银和硝酸锌固体。
设计实验步骤如下:
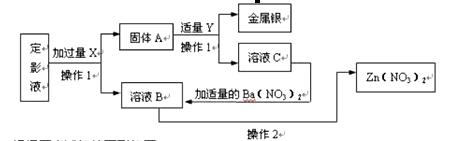
根据题意试解答下列问题:
( 1 )操作1 和2 的名称分别是 、 ;
( 2 ) X 为 ,Y 为 。(填化学式)
( 3 )加入适量的![]() 的目的是 ;
的目的是 ;
写出相关的反应方程式:
(14分)某校化学兴趣小组欲对食盐的用途进行探究,获得以下信息并对相关问题进行研究。
一、用途之一:作调味品。
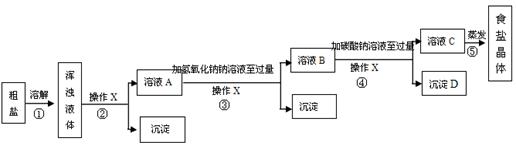
食盐的主要成份是NaCl, 通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
| 20℃时,一些物质的溶解度 | ||
| | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
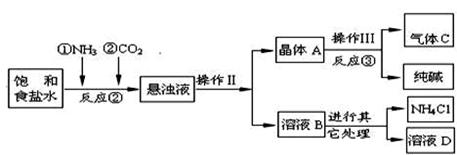
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com