
题目列表(包括答案和解析)
 实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):
实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):
| ||
| △ |
| ||
| △ |
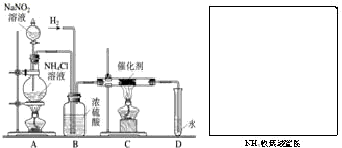 实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):
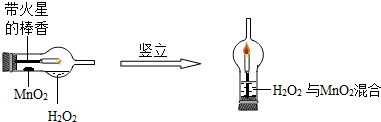
实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):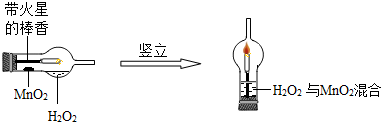
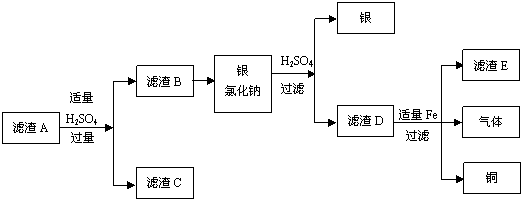
实验室废液中含有硝酸银、硝酸铜,实验小组利用稀硫酸和铁粉分离回收银和铜,设计如下方案。
先在废液中加入过量的铁粉,充分反应后过滤得到滤渣A,其成分为银、铜和铁。再对滤渣A按如下流程图处理:
①先在废液中加过量的铁粉,过量的目的是 。
Ⅰ、加快反应速度 Ⅱ、铁的金属活性较强 Ⅲ、使反应充分进行
②写出CuO与H2SO4反应的化学方程式 。
③滤液D中溶质的成分有 (填化学式)。
④含有硫酸亚铁的滤液有 (填框图中字母)。
⑤如果在过滤操作中发现滤液浑浊,在仪器清洁、滤纸未破损的前提下,你认为滤液的浑浊的原因可能是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com