
题目列表(包括答案和解析)
右下图是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。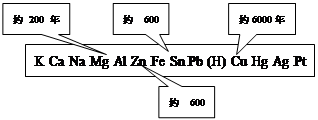
(1)选择编号填空:铝的利用比铜和铁晚得多,原因是 ;目前铝在多个领域替代易生锈的钢铁,其主要原因是 。
①铝很活泼②地壳中铝的含量高
③铝的硬度小且表面易生成致密的保护膜
(2)写出地壳中元素含量由多到少的前四位元素是 。
(3)若在CuSO4溶液中加入过量的铁粉和锌粉,最后得到的溶液中溶质的成分是 。
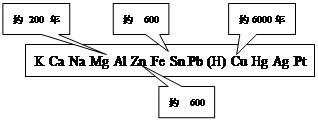
右下图是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。
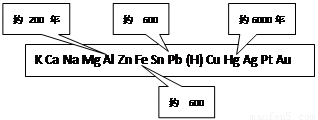
(1)选择编号填空:铝的利用比铜和铁晚得多,原因是 ;目前铝在多个领域替代易生锈的钢铁,其主要原因是 。
①铝很活泼 ②地壳中铝的含量高
③铝的硬度小且表面易生成致密的保护膜
(2)写出地壳中元素含量由多到少的前四位元素是 。
(3)若在CuSO4溶液中加入过量的铁粉和锌粉,最后得到的溶液中溶质的成分是 。
京京同学对金属活动性顺序等知识进行了研究。
(1)根据右图中的实验现象判断,稀盐酸里的A、B、C、D四种金属中,在金属活动性顺序里,位于氢后面的金属是(填字母) 。

(2)将甲、乙两种金属片分别放入硫酸铜溶液中,乙表面析出红色固体,甲没有明显现象。判断甲、乙、铜三种金属的活动性
由强到弱的顺序为 。
(3)查阅资料:金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.在下列①②中各写一个化学方程式,③中写出还原金属氧化物的方法。

(4)查阅资料:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO ↑ +4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成NO2,NO2是红棕色、有刺激性气味的有毒气体。
用右图所示实验装置进行实验,可以证明铜与稀硝酸反应生成的气体是NO。
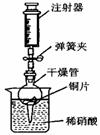
①检查装置的气密性:关闭弹簧夹,将干燥管放人带有水的烧杯中,若观察到 ,则表明该装置的气密性良好。
②按右图所示进行实验:打开弹簧夹,用注射器慢慢抽取干燥管内的气体,稀硝酸沿着干燥管慢慢上升,直到 ,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象: 。反应停止后,打开弹簧夹,用注射器抽取千燥管内的气体(事先已将注射器内原有的气体推出),关闭弹簧夹后取下注射器,并抽取一定量的空气,观察到气体变为红棕色。
③上述实验完成后,用足量NaOH溶液将气体吸收,其目的是
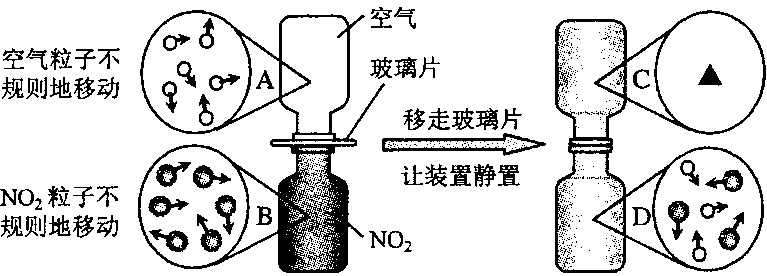
④下图是NO2气体和空气混合的实验示意图,观察图中A、B、D的表示方法,在C处画出相应的气体组成的粒子示意图。

京京同学对金属活动性顺序等知识进行了研究。
(1)根据右图中的实验现象判断,稀盐酸里的A、B、C、D
四种金属中,在金属活动性顺序里,位于氢后面的金属是(填 字母) 。
(2)将甲、乙两种金属片分别放入硫酸铜溶液中,乙表面析出红色固体,申没有明显现象。判断甲、乙、铜三种金属的活动性由强到弱的顺序为 。
(3)查阅资料:金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.在下列①②中各写一个化学方程式,③中写出还原金屑氧化物的方法。

(4)查阅资料:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO ↑ +4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成 N02,N02是红棕色、有刺激性气味的有毒气体。
用右下图所示实验装置进行实验,可以证明铜与稀硝酸反应生成的气体是NO。
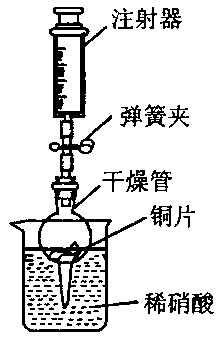
①检查装置的气密性:关闭弹簧夹,将干燥管放人带有水的烧杯
中,若观察到 ,
则表明该装置的气密性良好。
②按右图所示进行实验:打开弹簧夹,用注射器慢慢抽取干燥管
内的气体,稀硝酸沿着干燥管慢慢上升,直到 ,
停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象:
。
反应停止后,打开弹簧夹,用注射器抽取千燥管内的气体(事先已将注射器内原有的气体推出),关闭弹簧夹后取下注射器,并抽取一定量的空气,观察到气体变为红棕色。
③上述实验完成后,用足量NaOH溶液将气体吸收,其目的是
④下图是NO2气体和空气混合的实验示意图,观察图中A、B、D的表示方法,在C处 画出相应的气体组成的粒子示意图。
⑤在3.84 g Cu中加入100 g稀HNO3溶液,如恰好完全反应,计算生成NO的质量
(化学方程式见上)和反应前稀HNO3溶液中溶质的质量分数。 (请写出计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com