
题目列表(包括答案和解析)
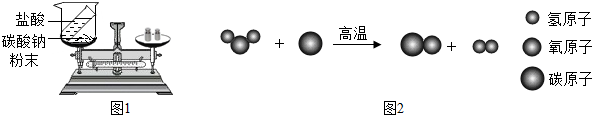
| 反应前后质量组别 | 甲组 | 乙组 | 丙组 |
| 盐酸与碳酸钠粉末反应前称量(g) | 85.3 | 82.8 | 86.5 |
| 盐酸与碳酸钠粉末反应后称量(g) | 85.3 | 80.6 | 87.8 |
| A.只含有碳元素 |
| B.只含有碳、氢两种元素 |
| C.碳元素质量分数为85.7% |
| D.碳、氢、氧元素质量比为6:1:8 |
一定质量的某物质充分燃烧,消耗了32g氧气,同时只生成44g二氧化碳和18g水,则该物质中
A.只含有碳元素 B.只含有碳、氢两种元素
C.碳元素质量分数为85.7% D.碳、氢、氧元素质量比为6:1:8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com