
题目列表(包括答案和解析)
为制备少量的氧气,某化学研究性小组开展了如下一系列研究工作。
[查阅资料]:通过查阅资料得知:双氧水、氯酸钾、高锰酸钾等物质在一定的条件下都可以分解产生氧气。其中,双氧水价格最低,在常温下就能够分解放出氧气,该反应无副产物;氯酸钾价格较高,分解较困难,且常伴有副产物;高锰酸钾价格较高,加热即可快速分解放出氧气。二氧化锰对上述三种物质的分解都能起催化作用。根据上述信息,该小组选择了双氧水和二氧化锰混合制取氧气。
[组装仪器]:选择下列实验仪器,安装实验装置,进行制备实验。
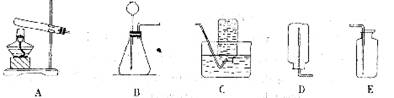
[实验操作]:进行实验完毕后,洗刷实验仪器,整理实验用品。
根据上述实验,请回答下列问题:
(1)要制取并收集一瓶氧气,应选择的实验装置是 (填写字母代号)。在组装好实验装置后,首先要进行 。
(2)有气体生成的化学反应,若在有限空间里发生时,如果反应过快,容易引起爆炸。你认为可以采取哪些措施预防爆炸?(列举一条)
(3)在选择药品时,除应考虑药品价格外,还应考虑哪些问题?(列举两条)
① ;
② 。
| ?温室气体还有哪些? ?人类的哪些活动造成大气温室气体增多? ?怎样才能减少大气中的温室气体,从而减缓地球的温室效应? | 什么是温室效应? 温室效应是怎么来的? 温室效应是由于大气中的大量二氧化碳、氟氯烃、甲烷、二氧化氮等温室气体(其中主要是CO2),像玻璃罩一样,紧紧地罩在我们的上空,使太阳照射在地球上的热量无法逸散,从而使气候圈增温的现象. 目前,产生温室效应主要同由于现代工业社会过多燃烧煤炭、石油和天然气以及森林大火等等这些燃料燃烧后放出大量的二氧化碳气体进入大气造成的 |  |
 |  |
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com