(2013?仪征市一模)水滑石化学式为:[Mg
6Al
2(OH)
16CO
3]?4H
2O(相对分子质量为602),是环保型阻燃剂.它受热时生成4种不同的氧化物,请写出该物质分解的化学方程式:
[Mg
6Al
2(OH)
16CO
3]?4H
2O
6MgO+Al
2O
3+CO
2↑+12H
2O
[Mg
6Al
2(OH)
16CO
3]?4H
2O
6MgO+Al
2O
3+CO
2↑+12H
2O
.
在医药上,水滑石还能作为抗酸药,作用于胃和十二指肠溃疡等,某研究型学习小组要测定一种市售的水滑石药片中水滑石的质量分数.
[查阅资料]水滑石与稀硫酸反应的化学方程式为:
[Mg
6Al
2(OH)
16CO
3]?4H
2O+9H
2SO
4═6MgSO
4+Al
2(SO
4)
3+CO
2↑+21H
2O.药片中除了水滑石外含有一定量的辅料--淀粉等物质.
[提出猜想]小华想将该药片放在空气中充分灼烧完成测定;小明想通过水滑石与硫酸反应原理来完成测定,请你参与探究.
[设计方案]他们设计了不同的实验方案.
小华的方案,称取10.0g市售的水滑石药片研磨成粉末置于通风橱中,充分灼烧至质量不再减少,再称量剩余固体的质量为6.1g,减少的质量即为二氧化碳和水的总质量,则可求的水滑石药片中水滑石的质量分数为
90.3
90.3
%.
小明的方案:
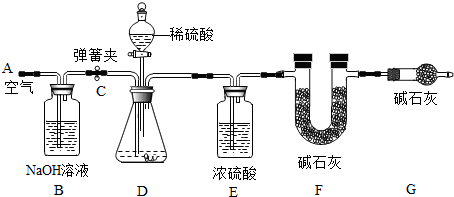
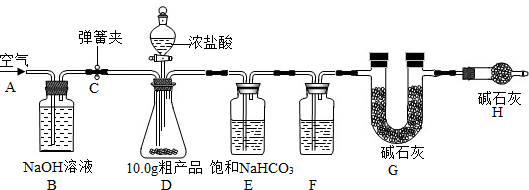
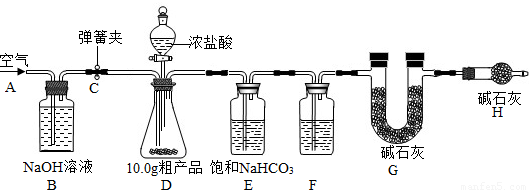
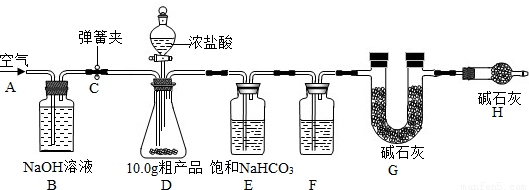
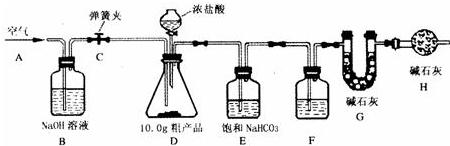
(1)小明设计了如图所示的实验装置.取10.0g市售的水滑石药片研磨成粉末,进行实验.
[说明]碱石灰是氧化钙和氢氧化钠固体的混合物.B装置中发生的化学方程式为
2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.
(2)操作步骤
①连接好装置,检查装置的气密性②打开弹簧夹C,在A处缓缓通入一段时间的空气③称量F的质量④关闭弹簧夹C,慢慢滴加稀硫酸至过量,直至D中无气泡冒出⑤打开弹簧夹C,再次缓缓通入一段时间空气⑥再次称量F的质量,得前后两次质量差为0.44g.
(3)问题探究
B、E装置的作用分别是
除去空气中的二氧化碳
除去空气中的二氧化碳
、
除去气体中混有的水蒸气
除去气体中混有的水蒸气
.若没有G装置,则测定的水滑石的质量分数会
偏大
偏大
(填“偏大”、“偏小”、“不变”).实验选用稀硫酸而不选用稀盐酸的理由是
用盐酸会使生成的二氧化碳中混有氯化氢气体
用盐酸会使生成的二氧化碳中混有氯化氢气体
.
(4)数据计算
根据实验数据,可求得水滑石药片中水滑石的质量分数为
60.2
60.2
%.(写出计算过程)
[方案评价]在上述实验方案中,你认为合理的实验方案是
小明
小明
(填小华或小明),另一个方案不合理的原因是
“药片中除了水滑石外含有一定量的辅料-淀粉等物质”中的淀粉受热会分解成水和二氧化碳而使结果偏大,
“药片中除了水滑石外含有一定量的辅料-淀粉等物质”中的淀粉受热会分解成水和二氧化碳而使结果偏大,
.