
题目列表(包括答案和解析)
(2007
,福州,14)某两种物质在一定条件下发生化学反应的微观示意如图(其中“ ”和“
”和“ ”分别表示两种不同的原子).
”分别表示两种不同的原子).
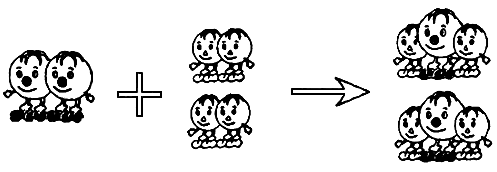
对上述反应,下列说法正确的是
?[
]|
A .反应物都是化合物 |
B .反应属于分解反应 |
|
C .生成物可能是氧化物 |
D .反应前后分子种类不变 |
14、某实验小组用含有各种必需营养元素的稀溶液培养大麦.试验分两组,一组在光照下,一组在黑暗中,48小时后测定几种离子的浓度.实验结束后溶液中的离子浓度与实验开始时的浓度之比如表表示(不考虑水分蒸发).由该实验作出的分析错误的是( )
|
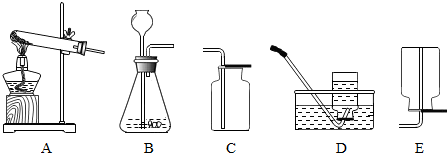
 、
、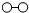 、
、 分别表示N2、H2、NH3.在催化剂表面(下图中
分别表示N2、H2、NH3.在催化剂表面(下图中 表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

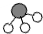
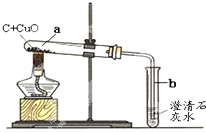 某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验.
某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验.| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案Ⅰ | 取少量固体物质于试管中,加足量稀硫酸充分振荡 | 溶液变成蓝色 | 固体中________ |
方案Ⅱ |  玻璃管中是反应后固体,通入足量空气 | 澄清石灰水________ | 固体中不含木炭 |
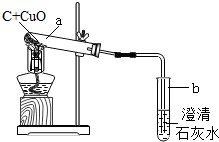 某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验.
某研究性小组在实验室用如图实验装置做木炭还原氧化铜的实验.
| ||
| ||
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案Ⅰ |
取少量固体物质于试管中,加足量稀硫酸充分振荡 | 溶液变成蓝色 | 固体中 氧化铜 氧化铜 |
方案Ⅱ |
 玻璃管中是反应后固体,通入足量空气 |
澄清石灰水 不变浑浊 不变浑浊 |
固体中不含木炭 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com